二酸化マンガンと塩酸の反応式は?【半反応式から解説】
高校化学において重要な用語として、合成法を適切に理解しておくことは重要です。
中でも、覚えておくべき反応の一つとして、二酸化マンガンと塩酸の反応式が挙げられます。
ここでは、二酸化マンガンと塩酸の反応式を添加したときに起こる反応について解説していきます。
・二酸化マンガンと塩酸の反応式を加えるた時の反応式
というテーマで解説していきます。
二酸化マンガンと塩酸の反応式を加えるた時の反応式
化学において化学反応式を扱う際には、ある物質とある物質を混ぜた際に、「各々が反応するものなのか」、もしくは「片方が触媒として反応するのか」を理解しておく必要があります。
例えば、二酸化マンガン(MnO2)と塩酸(濃塩酸)を混合し、加熱したときには、各々が以下のような化学反応式によって反応します。

この反応式はかなり頻出の式であるため、作り方について解説していきます。
まずは、各々の半反応式を記載していきます。二酸化マンガンの半反応式は以下の通りです。
二酸化マンガンの半反応式
まず、二酸化マンガンの半反応式は以下の通りとなります。

この式の作り方について、順を追って確認していきます。二酸化マンガンは酸化剤として働くために、自身は還元されます(酸化数が下がる)。ここで、MnO2がMn2+になることを理解しておきましょう。
この式を書いた後に、左辺と上辺のOの数が一致するように、2H2Oを記載します。
すると、左辺に水素原子H+を4つ分足して、一致させます。続いて、両辺の電荷の大きさが一致するように電子を足していくと上式ができるわけです。
基本的に半反応式の作り方は、反応するものと生成物を覚えておけば上の手順をたどることで、対応できることを理解しておきましょう。
塩酸の半反応式
続いて、塩酸の半反応式を考えていきます。
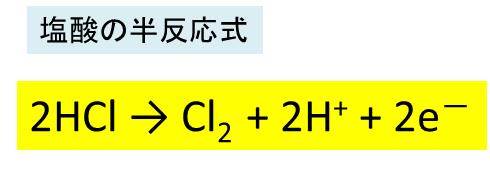
こちらでも同様に式の作り方について、順を追って確認していきます。このとき、塩酸は還元剤として働くために、自身は酸化されます(酸化数が上がる)。なお、HClからCl2が生成されることを覚えてしておきましょう。
この式を書いた後に、左辺と上辺のHの数が一致するように、右辺2H+を記載します。
続いて、両辺の電荷の大きさが一致するように電子(2e-)を足していくと上式ができるわけです。
二酸化マンガンと塩酸の反応式
今回は二つの式の電子の数に着目していきます。今回は2e-で同じであるため、そのまま足し合わせるといいです。
・MnO2 + 4H+ + 2e- → Mn2+ + 2H2O
・2HCl → Cl2 + 2H+ + 2e-
すると、以下のようになります。
・MnO2 + 2H + 2HCl → Mn2+ + 2H2O + Cl2 後は両辺に2Cl-を追加すると、先にも述べた反応式となるわけです。
以下で改めて二酸化マンガンと塩酸(塩化水素)の反応式を記載していきます。

関連記事
塩酸の化学式、分子式、電子式、構造式、分子量は?
酸化剤、還元剤とは?
二酸化マンガンと塩酸の反応式は?【半反応式から解説】 関連ページ
- イオンとはそもそも何のこと?その1 イオン発見の歴史と原子の構造と原子番号、質量数
- 酸化とは?還元とは?酸化還元の定義その1、その2
- 酸化還元の定義その3とまとめ
- 電池とは?ボルタ電池の構成と反応
- ダニエル電池の構成・仕組み・反応式は?正極・負極の反応は?素焼き板の役割は?
- イオン化傾向とは?
- 【手計算・Excel】pHとは?計算方法は?
- 同位体の存在比とは?計算問題を解いてみよう【銅や塩素の質量】
- 分子量の求め方 アンモニア・メタン・尿素などの分子量を計算してみよう【演習問題】
- 原子量・分子量・式量の違いは?
- アレニウス・ブレンステッド・ルイスの酸・塩基の定義と違いは?
- 電池の電極の質量変化を計算してみよう【ダニエル電池の質量変化】
- 絶対質量と相対質量 相対質量の計算方法(絶対質量との変換)
- ルシャトリエの法則(原理)とは?
- 電気分解とは?塩化銅水溶液(CuCl2)における電気分解の反応式 陽極・陰極での反応式 陽極、陰極、正極、負極の違いと覚え方(見分け方)
- 水の電気分解の仕組み・反応式 陽極・陰極での反応式 水酸化ナトリウムを入れる理由は?
- ヘスの法則と熱化学方程式の関係 計算問題を解き、反応熱を求めてみよう【演習問題】
- ボルンハーバーサイクルとは?イオン結晶の格子エネルギー(格子エンタルピー)を計算してみよう
- 同位体と同素体の違いは?
- 物質量とモル質量の違いは?計算問題を解いてみよう【演習問題】
- 乾燥剤と気体の酸性・塩基性・中性とは?
- 気体の酸性度 酸性気体、中性気体、塩基性(アルカリ性)気体
- 潮解性・吸湿性・脱水性の違いは?
- 生石灰と消石灰とは?分子式(化学式)や用途の違い 生石灰と水との反応式は?
- ソーダ石灰の性質や塩基性(アルカリ性)の乾燥剤としての役割(アンモニアや二酸化炭素は吸収できる?)
- 単体、化合物、純物質、混合物の定義や違い
- 気体の水溶性と気体の収集方法(上方置換、下方置換、水上置換)
- 塩化水素が水に溶けやすい理由は?
- アンモニアが水に溶けやすい理由は?
- 「原子量・分子量・式量」とモル質量との違い
- 物質量(モル:mol)とアボガドロ数の違いや関係は? 計算問題を解いてみよう
- コロイドの性質 チンダル現象・ブラウン運動・電気泳動とは?
- クメン法とは?クメンヒドロペルオキシドを経由してフェノールを合成する方法
- 過酸化水素に二酸化マンガンを加えた時の反応式は?
- 疎水コロイド・親水コロイド・保護コロイド 凝析と塩析とは?
- 十酸化四リンの化学式、分子式(P4O10)、構造式は? 十酸化四リンと五酸化二リンの違いは?
- 乾燥剤である十酸化四リンが使用できない物質は? 潮解性や脱水作用を持つのか?
- リンの同素体 黄リンと赤リンの違いは?
- 分子結晶と共有結晶(共有結合性結晶)の違いは?
- 酸素の同素体 酸素とオゾンの違いは?
- 炭素の同素体 黒鉛(グラファイト)・ダイヤモンド・フラーレンの違いは?
- 浸透圧とファントホッフの式 計算問題を解いてみよう【演習問題】
- イオン結晶とイオン結合 イオン結晶の融点・沸点・電気伝導性などの性質
- 金属結晶と金属結合 金属結晶の融点・沸点・電気伝導性などの性質
- 自由電子と価電子の違いは?
- 共有結晶(共有結合結晶)と共有結合 共有結晶の融点・沸点・電気伝導性などの性質
- 分子結晶と分子間力 分子結晶の融点・沸点・電気伝導性などの性質
- 配位結合とは?配位結合の強さと矢印の書き方 共有結合・イオン結合・水素結合との違いは?
- 金属の配位結合と錯イオン(錯体) 中心金属、配位子、配位数とは?
- 食塩水の電気分解における電極での反応式(イオン式) 陽極で塩素が発生し、陰極で水素が発生する理由