【緩衝作用】酢酸の緩衝溶液のpHを計算してみよう【酢酸の解離平衡時の平衡定数】
電気化学的な技術を用いているめっきですが、めっき浴とよばれるめっきを行うために準備する液体があります。この液体にめっきさせたいものを入れ、被膜を形成することが基本です。
めっきではpHや温度条件などで、めっきの良し悪しが決まるためにその管理をきちんと行うことが大事です。
特にpHの変化を抑えるためには、めっき浴にはほう酸、りん酸などの有機酸が添加されています。
このように、pHの変化を抑制する作用のことを緩衝作用とよびます。
ここでは、緩衝作用や酢酸の電離平衡(解離平衡)時の平衡定数、pHの計算方法に関する以下の内容を解説していきます。
・緩衝作用とは?
・酢酸(CH3COOH)と酢酸ナトリウム(CH3COONa)の解離(電離)と緩衝作用
・酢酸の緩衝溶液のpHを計算してみよう【酢酸の解離平衡時の平衡定数】
というテーマで解説していきます。
緩衝作用とは?
緩衝作用とはpHとの関わりが強く、ある溶液に添加剤を加えることによってpHの変化を抑える作用のことを指します。pHの変化を抑制することは、酸塩基平衡を保つことともいえます。
また、このような緩衝作用をもつ溶液のことを緩衝溶液とよびます。緩衝溶液として、有名なものの例としては、酢酸と酢酸ナトリウムの組み合わせであったり、アンモニアと塩化アンモニウムの組み合わせがあります。
つまり、電離度が低い酸性の溶液(弱酸)とその塩の組み合わせであったり、同様に電離度が低いアルカリ性の溶液(弱塩基)とその塩の組み合わせがあると、この緩衝作用が表れます。
以下で緩衝作用について、具体例を交えて解説していきます。
関連記事
pHとは?計算方法とは?
めっきとは?めっきの原理と種類
有機酸とは?
酢酸(CH3COOH)と酢酸ナトリウム(CH3COONa)の解離(電離)と緩衝作用
酢酸の場合は以下のような電離平衡を形成しています。
CH3COOH ⇄ CH3COO- + H+ が成立します。酢酸は弱酸であるために、位置が完全に電離しているわけではなく(電離度が1でない)、一部のみが電離しています。
一方で、酢酸ナトリウムは以下のような電離平衡となります。
CH3COONa ⇄ CH3COO- + Na+ となります。こちらは、塩であるため基本的にほぼ完全に電離しています。つまり、CH3COO-が大量にあるといえます。
よって、最初に挙げた酢酸の電離平衡において、CH3COO-が大量にあるために、ルシャトリエの法則により平衡が左のCH3COOHに偏っています。つまり、ただでさえ電離度が高くない、酢酸の電離度がさらに低下しているといえます。
そして、何らかの副反応がおこりプロトン濃度(H+)が高まったとします。つまり酸性度が強くなるとします。このときに、多量にあるCH3COO- + H+ → CH3COOHの反応が起こるため、酸性度が高くなりません。
逆に何かしらの望んでいない反応により、OH-の濃度が高まったとします。このときは、CH3COOH + OH- → CH3COOH + H2O という反応が起こるため、こちらもpHが変化しません。
このようなメカニズムから緩衝溶液では、緩衝作用がおこることによって、pHの変化が抑制されるという仕組みになっています。
また、先の例のように同じような物質やイオンで似たようなものから構成されるために、pH抑制することができました。似たような構成であるため、両式においてCH3COO-が関係することが要因です。このように、共通のイオンが反応に関わっており、共通のイオンの発生が抑えられていることを共通イオン効果ともよびます。
関連記事
pHとは?計算方法とは?
めっきとは?めっきの原理と種類
有機酸とは?
酢酸の緩衝溶液のpHを計算してみよう【酢酸の解離平衡時の平衡定数】
例題
酢酸の電離定数をKa=10^-4.7mol/Lとして以下の例題をといてみましょう。
CH3COOHの濃度が0.15mol/Lであり、かつCH3COO-の濃度も0.15mol/Lである、200mlの溶液があるとします。
ここで、H2SO4を0.003mol/LとかしたときのpHの変化を考えていきましょう。
体積変化は無視できるとします。
解答
典型的な緩衝溶液におけるpH計算の問題です。
反応前、反応量、反応後の各々濃度を表にまとめるとわかりやすいです。以下の通りです。
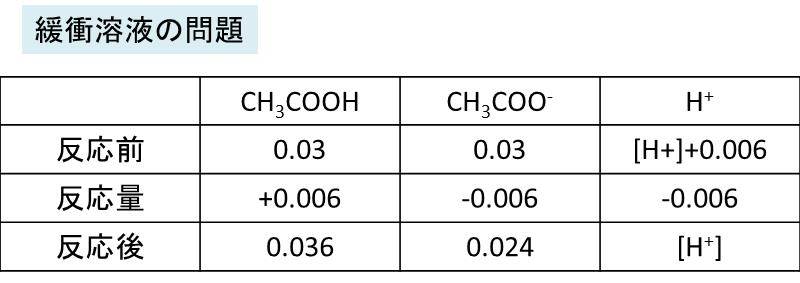
これを緩衝溶液における平衡定数の式に当てはめ、その値を比較することで、水素イオン濃度を算出します。
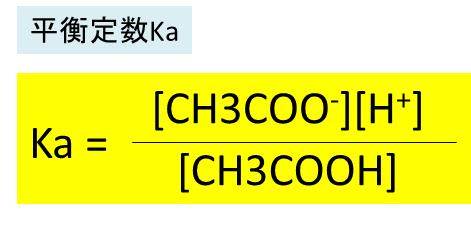
この式に代入して、10^-4.7mol = 0.0024 × [H+] / 0.036 をときます。
すると [H+]=約3 ×10^-4 mol/Lとなります。pHの定義より、-log10 (3×10-4)より、4-0.477=3.523となります。
関連記事
pHとは?計算方法とは?
めっきとは?めっきの原理と種類
有機酸とは?
【緩衝作用】酢酸の緩衝溶液のpHを計算してみよう【酢酸の解離平衡時の平衡定数】 関連ページ
- エネルギー変換
- 化学変化の基礎(エンタルピー、エントロピー、ギブズエネルギー)
- 反応ギブズエネルギーと標準生成ギブズエネルギー
- 化学平衡と化学ポテンシャル、活量、平衡定数○
- 電圧とギブズエネルギーの関係○
- 化学ポテンシャルと電気化学ポテンシャル、ネルンストの式○
- ネルンストの式の導出
- 【演習問題】ネルンストの式を使用する問題演習をしよう!
- 電池反応に関する標準電極電位のまとめ(一覧)
- 標準電極電位とは?電子のエネルギーと電位の関係から解説
- 標準電極電位の表記例と理論電圧(起電力)の算出【電池の起電力の計算】
- 標準電極電位と金属の電子状態○
- 電池内部の電位分布、基準電極に必要なこと○
- 基準電極の種類
- 電気二重層、表面電荷と電気二重層モデル
- 電気化学の測定方法 -三電極法-
- サイクリックボルタンメトリーの原理と測定結果の例
- サイクリックボルタンメトリーにおける解析方法
- LSVの原理と測定結果の例
- クロノアンぺロメトリ―の原理と測定結果の例
- クロノポテンショメトリ―の原理と測定結果の例
- 電荷移動律速と拡散律速(電極反応のプロセス)○
- リチウムイオン電池と等価回路(ランドルス型等価回路)
- リチウムイオン電池と交流インピーダンス法【インピーダンスの分離】
- 【拡散律速時のインピーダンス】ワールブルグインピーダンスとは?限界電流密度とは?【リチウムイオン電池の抵抗成分】
- 電解質の電気抵抗、電気伝導率
- イオンの移動度とモル伝導率 輸率とその計算方法は?
- イオン強度とは?イオン強度の計算方法は?
- 電子授受平衡と交換電流、交換電流密度○
- Butler-Volmerの式(過電圧と電流の関係式)○
- Tafel式とは?Tafel式の導出とTafelプロット○
- 【演習】アレニウスの式から活性化エネルギーを求める方法
- 活性化エネルギー詳細
- 加速劣化試験と電池部材の耐食性評価
- 腐食とは?腐食の種類と電位-pH図
- めっきとは?めっきの役割と種類
- 自己触媒めっきと自己触媒
- 【演習問題】電流効率とは?電流効率の計算方法【リチウムイオン電池部材のめっき】
- 隙間腐食(すきま腐食)の意味と発生メカニズム
- 電食・ガルバニック腐食・異種金属腐食
- 濃淡電池の原理・仕組み 酸素濃淡電池など
- 浸透探傷試験(レッドチェック)
- ファラデーの法則とは?ファラデー電流と非ファラデー電流とは?
- ド・ブロイの物質波とハイゼンベルグの不確定性原理
- 波動関数と電子の存在確率(粒子性と波動性の結び付け)
- シュレーディンガー方程式とは?波の式からの導出
- 波の式を微分しシュレーディンガー方程式を導出
- 井戸型ポテンシャルの問題とシュレーディンガー方程式の立式と解
- オイラーの公式と導出
- 光と電気化学 基底状態と励起状態 蛍光とりん光 ランベルト-ベールの式
- 光束・光度・輝度の定義と計算方法【演習問題】
- 電磁波の分類 波長とエネルギーの関係式 1eVとは?eV・J・Vの変換方法【計算問題】
- 光と電気化学 励起による酸化還元力の向上
- 溶解度積と沈殿平衡 導出と計算方法【演習問題】
- 再配向エネルギーと活性化エネルギー
- 内圏型と外圏型電子移動の違い
- pHメーター(pHセンサー)の原理・仕組みは?pHメーターとネルンストの式
- ガスセンサー(固体電解質)の原理とは?ネルンストの式との関係は?
- オリゴマーとは?ポリマーとオリゴマーの違いは?数平均分子量と重量平均分子量の求め方【演習問題】
- 面心立方格子、体心立方格子、ミラー指数とは?【リチウムイオン電池の正極材の結晶構造は】
- アタクチックポリマー、イソタクチックポリマー、シンジオタクチックポリマーの違いは?【ポリマーのタクチシチ―】
- おすすめの電気化学の参考書
- 【電流密度】電流密度と電流の関係を計算してみよう【演習問題】
- ギブズの相律とは?F=C-P+2とは?【演習問題】
- 状態関数と経路関数 示量性状態関数と示強性状態関数とは?
- 定容熱容量(Cv)と定圧熱容量(CP)とは?違いは?
- 分子間相互作用
- 理想気体と実在気体の状態方程式(ファンデルワールスの状態方程式) 排除体積とは?排除体積の計算方法
- オクテット則
- 電子軌道 s軌道・p軌道とは?
- 混合エントロピー 計算と導出方法は?
- 錯体・キレート 錯体平衡の計算問題を解いてみよう【演習問題】
- 「速度論的に安定」と「熱力学的に安定」
- 触媒の仕組みと化学反応
- 分配平衡と分配係数・分配比 導出と計算方法【演習問題】
- 塩橋の役割と入れる理由
- レナードジョーンズポテンシャル 極小値の導出と計算方法【演習問題】
- ルイス酸とルイス塩基の定義 見分け方と違い
- 膜電位の定義と計算方法
- トルートンの規則 トルートンの式
- 化学におけるクラスターとは
- 結晶粒界(粒界)の定義と粒界腐食
- 化学におけるキャラクタリゼーションとは
- 化学におけるバルクとは?バルク水とは
- 電気化学における活性・不活性とは?活性電極と不活性電極の違い
- 1eVは熱エネルギー(温度エネルギー)に換算するとどのくらいの大きさになるのか
- 物質の相図(状態図)と物質の三態の関係 水の状態図の見方 蒸発・凝縮・融解・凝固・昇華・凝結とは? 三重点と臨界点とは?
- プランク定数とエイチ÷2πの定数(エイチバー:ディラック定数)との関係
- 活量係数とは?活量係数の計算問題をといてみよう【活量と活量係数の関係】
- 光触媒である二酸化チタンの原理や用途
- 水素脆性(ぜいせい)、水素脆化の意味と発生の原理は?ベーキング処理とは?
- 波数と波長の変換(換算)の計算問題を解いてみよう
- 波長と速度と周波数の変換(換算)方法 計算問題を解いてみよう
- 波数とエネルギーの変換方法 計算問題を解いてみよう