定容熱容量(Cv)と定圧熱容量(CP)とは?違いは?
電気化学を理解する上で、「エネルギー変換の仕組み」や「エンタルピー・エントロピー・ギブズエネルギー」といったエネルギーの相互変換の基礎となる式について理解することは大事です。
各エネルギーの中でも、熱エネルギーに関する用語として、「定容熱容量(CV)」と「定圧熱容量(CP)」とよばれるものがあります。定容熱容量(CV)と定圧熱容量(CP)の定義やその違いについて知っていますか?
ここでは、定容熱容量(CV)と定圧熱容量(CP)の定義やその違いについて解説していきます。
・そもそも熱容量とは?
・定容熱容量(CV)の導出
・定圧熱容量(CP)の導出 CpとCVの違いは?
・定容熱容量(Cv)と定圧熱容量(Cp)の計算問題を解いてみよう【演習問題】
というテーマで解説していきます。
そもそも熱容量とは?
熱容量とは、ある物質のあたたまりにくさを表している指標です。熱容量の定義としては、ある物質を1℃(1K)あたためるために必要な熱量(エネルギー)といえます。
つまり、熱容量が大きいほどあたたまりにくい物体であるといえます。
熱容量には種類があり、定容熱容量と定圧熱容量があります。
言葉の通り、定容熱容量とは定容条件、つまり体積が一定の条件下での物体のあたたまりにくさ(熱容量)です。CVつまり、constant volumeの略です。
一方で、定圧熱容量とは、定圧条件下、つまり圧力が一定の条件下での熱容量のことを指します。CPつまり、constant pressureの略です。
(※ちなみに、熱容量と比熱には深い関係があり、こちらで詳しく解説しています。)
以下で一つずつ確認していきます。
関連記事
状態関数とは?
エンタルピー、エントロピー、ギブズエネルギーとは?
熱容量と比熱の関係・違いは?
定容熱容量(CV)の導出
まずは、より簡単に導出できる定容熱容量の方の導出から行っていきましょう。
言葉の通り定容の熱容量を考えるときには、体積が一定の系を考えていきます。
以下のようなイメージです。
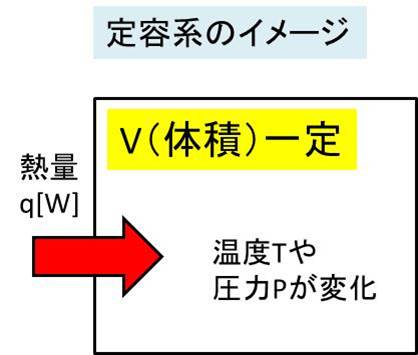
つまり、内部エネルギーの変化に着目しますと、外部への仕事Wは無し(=0)といえます。外部から形に与えた熱エネルギーqがそのまま、系の中の物質の温度変化の熱量に相当するといえます。
これを式にすると、Cv ⊿ T = Q という計算式が成り立ちます。このCvが定容熱容量を表しています。
もしくはq = ∫ Cv dT とも記載できます。

定容変化では、熱量の変化と内部エネルギーの変化が等しくなります。そのため、Cv = ⊿U(内部エネルギー) / ⊿T(温度変化)ともかけます。
1molあたりの定容熱容量のことを定容モル熱容量と呼びます。
関連記事
状態関数とは?
エンタルピー、エントロピー、ギブズエネルギーとは?
熱容量と比熱の関係・違いは?
定圧熱容量(CP)の導出 CpとCVの違いは?
次に、定圧熱容量(Cp)の導出を行います。
言葉の通り定圧の熱容量を考えるときには、圧力Pが一定の系を考えていきます。そのため、系に熱量を与えると体積が変動し、外部に仕事をすることになります。
以下のようなイメージです。
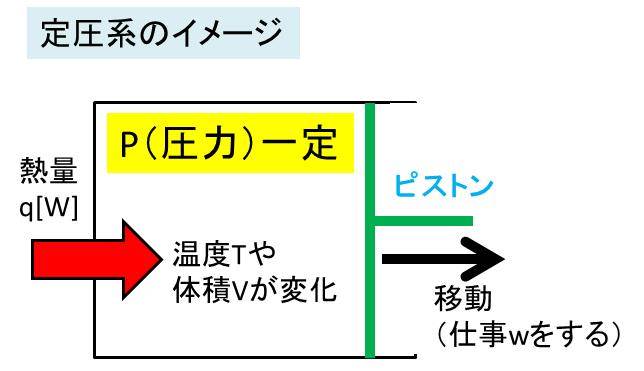
ここで、定圧条件下では、仕事分があるため結局はエンタルピー変化を考えればいいです。
よって、Cp ⊿ T = ⊿H という計算式が成り立ちます。このCpが定容熱容量を表しています。

ここで、⊿H= ⊿U + p⊿Vで表すことができます。ここで、⊿U / ⊿T =Cvであることを使用しましょう。
すると、この両辺を⊿Tでわると、Cp = Cv + p⊿V/⊿T となります。
ここで最後の項は、1molであれば気体の状態方程式pv=RTより、Rとなります。
これがCpとCvの差の公式といえます。
つまり、Cpの方が仕事分が若干大きな値となります。
関連記事
状態関数とは?
エンタルピー、エントロピー、ギブズエネルギーとは?
熱容量と比熱の関係・違いは?
ファンデルワールスの状態方程式とは?
定容熱容量(Cv)と定圧熱容量(Cp)の計算問題を解いてみよう【演習問題】
例題
定容下条件において、可変しない容器内に物質を2mol充填するとします。
このときに、外部から100Jの熱量を与えたときに、5K温度が変化したとします。
このときの、定容モル熱容量と定圧のモル熱容量の計算しましょう。
解答
以下のような求め方で計算できます。
定容モル熱容量は定義に従い、Cv = 100 / 2 / 5 =10[J/K/mol] となります。
一方定圧熱容量Cp = Cv + R = 10 + 8.31 =18.31[J/K/mol] となります。
どちらのモル熱容量の単位は[J/K/mol] となることに気を付けましょう。
関連記事
状態関数とは?
エンタルピー、エントロピー、ギブズエネルギーとは?
熱容量と比熱の関係・違いは?
ファンデルワールスの状態方程式とは?
定容熱容量(Cv)と定圧熱容量(CP)とは?違いは? 関連ページ
- エネルギー変換
- 化学変化の基礎(エンタルピー、エントロピー、ギブズエネルギー)
- 反応ギブズエネルギーと標準生成ギブズエネルギー
- 化学平衡と化学ポテンシャル、活量、平衡定数○
- 電圧とギブズエネルギーの関係○
- 化学ポテンシャルと電気化学ポテンシャル、ネルンストの式○
- ネルンストの式の導出
- 【演習問題】ネルンストの式を使用する問題演習をしよう!
- 電池反応に関する標準電極電位のまとめ(一覧)
- 標準電極電位とは?電子のエネルギーと電位の関係から解説
- 標準電極電位の表記例と理論電圧(起電力)の算出【電池の起電力の計算】
- 標準電極電位と金属の電子状態○
- 電池内部の電位分布、基準電極に必要なこと○
- 基準電極の種類
- 電気二重層、表面電荷と電気二重層モデル
- 電気化学の測定方法 -三電極法-
- サイクリックボルタンメトリーの原理と測定結果の例
- サイクリックボルタンメトリーにおける解析方法
- LSVの原理と測定結果の例
- クロノアンぺロメトリ―の原理と測定結果の例
- クロノポテンショメトリ―の原理と測定結果の例
- 電荷移動律速と拡散律速(電極反応のプロセス)○
- リチウムイオン電池と等価回路(ランドルス型等価回路)
- リチウムイオン電池と交流インピーダンス法【インピーダンスの分離】
- 【拡散律速時のインピーダンス】ワールブルグインピーダンスとは?限界電流密度とは?【リチウムイオン電池の抵抗成分】
- 電解質の電気抵抗、電気伝導率
- イオンの移動度とモル伝導率 輸率とその計算方法は?
- イオン強度とは?イオン強度の計算方法は?
- 電子授受平衡と交換電流、交換電流密度○
- Butler-Volmerの式(過電圧と電流の関係式)○
- Tafel式とは?Tafel式の導出とTafelプロット○
- 【演習】アレニウスの式から活性化エネルギーを求める方法
- 活性化エネルギー詳細
- 加速劣化試験と電池部材の耐食性評価
- 腐食とは?腐食の種類と電位-pH図
- めっきとは?めっきの役割と種類
- 自己触媒めっきと自己触媒
- 【演習問題】電流効率とは?電流効率の計算方法【リチウムイオン電池部材のめっき】
- 隙間腐食(すきま腐食)の意味と発生メカニズム
- 電食・ガルバニック腐食・異種金属腐食
- 濃淡電池の原理・仕組み 酸素濃淡電池など
- 浸透探傷試験(レッドチェック)
- ファラデーの法則とは?ファラデー電流と非ファラデー電流とは?
- ド・ブロイの物質波とハイゼンベルグの不確定性原理
- 波動関数と電子の存在確率(粒子性と波動性の結び付け)
- シュレーディンガー方程式とは?波の式からの導出
- 波の式を微分しシュレーディンガー方程式を導出
- 井戸型ポテンシャルの問題とシュレーディンガー方程式の立式と解
- オイラーの公式と導出
- 光と電気化学 基底状態と励起状態 蛍光とりん光 ランベルト-ベールの式
- 光束・光度・輝度の定義と計算方法【演習問題】
- 電磁波の分類 波長とエネルギーの関係式 1eVとは?eV・J・Vの変換方法【計算問題】
- 光と電気化学 励起による酸化還元力の向上
- 溶解度積と沈殿平衡 導出と計算方法【演習問題】
- 再配向エネルギーと活性化エネルギー
- 内圏型と外圏型電子移動の違い
- pHメーター(pHセンサー)の原理・仕組みは?pHメーターとネルンストの式
- ガスセンサー(固体電解質)の原理とは?ネルンストの式との関係は?
- オリゴマーとは?ポリマーとオリゴマーの違いは?数平均分子量と重量平均分子量の求め方【演習問題】
- 面心立方格子、体心立方格子、ミラー指数とは?【リチウムイオン電池の正極材の結晶構造は】
- アタクチックポリマー、イソタクチックポリマー、シンジオタクチックポリマーの違いは?【ポリマーのタクチシチ―】
- おすすめの電気化学の参考書
- 【電流密度】電流密度と電流の関係を計算してみよう【演習問題】
- ギブズの相律とは?F=C-P+2とは?【演習問題】
- 状態関数と経路関数 示量性状態関数と示強性状態関数とは?
- 分子間相互作用
- 理想気体と実在気体の状態方程式(ファンデルワールスの状態方程式) 排除体積とは?排除体積の計算方法
- オクテット則
- 【緩衝作用】酢酸の緩衝溶液のpHを計算してみよう【酢酸の解離平衡時の平衡定数】
- 電子軌道 s軌道・p軌道とは?
- 混合エントロピー 計算と導出方法は?
- 錯体・キレート 錯体平衡の計算問題を解いてみよう【演習問題】
- 「速度論的に安定」と「熱力学的に安定」
- 触媒の仕組みと化学反応
- 分配平衡と分配係数・分配比 導出と計算方法【演習問題】
- 塩橋の役割と入れる理由
- レナードジョーンズポテンシャル 極小値の導出と計算方法【演習問題】
- ルイス酸とルイス塩基の定義 見分け方と違い
- 膜電位の定義と計算方法
- トルートンの規則 トルートンの式
- 化学におけるクラスターとは
- 結晶粒界(粒界)の定義と粒界腐食
- 化学におけるキャラクタリゼーションとは
- 化学におけるバルクとは?バルク水とは
- 電気化学における活性・不活性とは?活性電極と不活性電極の違い
- 1eVは熱エネルギー(温度エネルギー)に換算するとどのくらいの大きさになるのか
- 物質の相図(状態図)と物質の三態の関係 水の状態図の見方 蒸発・凝縮・融解・凝固・昇華・凝結とは? 三重点と臨界点とは?
- プランク定数とエイチ÷2πの定数(エイチバー:ディラック定数)との関係
- 活量係数とは?活量係数の計算問題をといてみよう【活量と活量係数の関係】
- 光触媒である二酸化チタンの原理や用途
- 水素脆性(ぜいせい)、水素脆化の意味と発生の原理は?ベーキング処理とは?
- 波数と波長の変換(換算)の計算問題を解いてみよう
- 波長と速度と周波数の変換(換算)方法 計算問題を解いてみよう
- 波数とエネルギーの変換方法 計算問題を解いてみよう