電解液(溶媒)の材料化学
いまでは、スマホ向けバッテリーや家庭用蓄電池、電気自動車用搭載電池としてリチウムイオン電池が主に採用されています。
リチウムイオン電池は他の二次電池と比較しても、高電圧、高エネルギー密度、高出力、長寿命などのメリットがあります。
これらのメリットは主にリチウムイオン電池の内部抵抗が低いことが挙げられます。
内部抵抗の低さを実現するための要因の一つとして、電解液の設計(電解液に求められる特性を満たすこと)が挙げられます。
リチウムイオン電池の電解液は通電時、正極、負極間のリチウムイオンの移動、受け渡しをする役割を持っています。
リチウムイオン電池における 電解液は溶媒にLi含有塩を溶かしたものであるため、溶媒と塩両方を考慮して設計する必要があります(塩(LiPF6)に求められる特性はこちらで解説しています)。
ここでは、電解液の溶媒に求められる特性について解説しています。
・電解液の溶媒に求められる特性 電位窓が広いこと
・電解液の溶媒に求められる特性 電気伝導率が広いこと
・電解液の溶媒に求められる特性 良質なSEIを形成すること
というテーマで解説しています。
(リチウムイオン電池の唯一の課題としては、安全性が低いことがあります。最近急増のリチウムイオン電池の発火事故のメカニズムや発火時の対処・消火方法についてはこちらで解説しています。)
電解液の溶媒に求められる特性 電位窓が広いこと
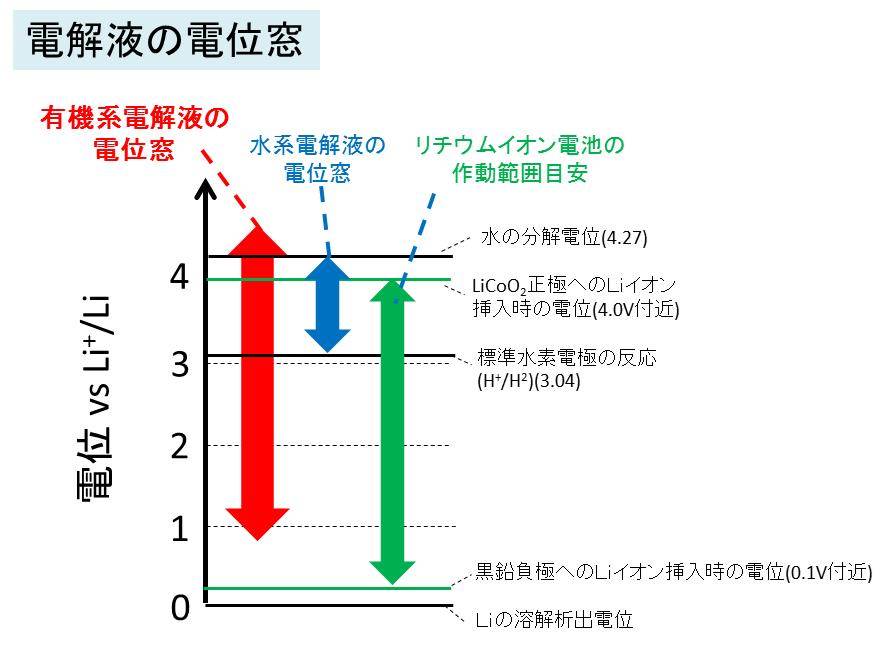
実用化されている電池では、溶媒は水系ではなく有機溶剤系が使用されています。
これは下図のよう、有機溶媒は水系溶媒と比べて、電位窓(分解されずに安定して使用できる電位の範囲)が広いからです。
リチウムイオン電池では使用している3V~4V付近と他の電池と比べて高い電圧で動作します、
そのため、高い作動電圧に耐えられる電解液でないと分解されて、電池として機能しなくなります。これがリチウムイオン電池の溶媒に有機溶媒が使用されている理由です。
特に、正極にて充電時に酸化反応が起こる方向(電位が上げる方向)では電位窓の上限が高いことが強く求められます。
ただ、負極に黒鉛を使用する場合は、電位窓の下限が1V弱程度と黒鉛の作動電位よりも高くても問題ないです(還元側では電位窓をこえていても大丈夫)。
これは炭素系材料を使用した場合は、初回充電時に電解液が還元的に分解されSEI(固体電解質相)と呼ばれる被膜ができ、Liイオン伝導は保ちつつ、電解液の分解が大きく抑制されるという便利な機能を持っているためです。
関連記事
リチウムイオン電池の構成材料の危険物の分類
SEI(固体電解質相)とは?
エネルギー密度とは?
家庭用蓄電池設置のメリット・デメリット
電気自動車、プラウインハイブリッド車の違い
酸化、還元とは?アノード、カソードとは?
電解質の塩(LiPF6)に求められる特性
電解液の添加剤とは(VCやFEC)
電解液の溶媒に求められる特性 電気伝導率が高いこと
リチウムイオン電池の作動電圧は、SOC-OCV曲線の形と内部抵抗により決まります。
電解液の塩に求められることに解説しましたが、低抵抗な電池を設計するには、電解液の電気伝導率が高いことが求められます。
電気伝導率は下記の式であらわされます。

電気伝導度を高める要素として、
①イオンの解離能を上げること(式中の濃度cが上がる)
②移動度を上げること(式中の移動度uが上がる)
があります。
溶媒からのアプロ―チとしては、
①イオン解離能(濃度)を上げるための比誘電率が大きい材料
②移動度を上げるための粘度が低い材料
を混ぜることで最適化されます。
①比誘電率の高い材料を入れる理由
比誘電率を上げるとなぜイオンが解離しやすいのでしょうか?
溶媒の比誘電率とあるイオンの溶媒和のギブズエネルギーの関係を表したボルンの式で説明できます。

上式から、電荷zが大きく、イオン半径rが小さく、比誘電率εrが大きいほど⊿G(溶媒和のギブズエネルギー)
が絶対値が大きい負の値を取ることになります。
ギブズエネルギーは負であると反応が自発的に起こります。
(速度論的に反応が非常に遅い場合を除きます。)
また、負でその絶対値が大きいということは自発的に反応が進むための推進力が大きいということであり、
比誘電率が大きいほど溶媒和が進む、つまりイオンが解離しやすくなります。
比誘電率が高く、電位窓が広い材料にエチレンカーボネート(EC)やプロピレンカーボネート(PC)等の環状のカーボネート系材料が挙げられます。
これらを使用することで比誘電率を高く出来るのですが、比誘電率が高い溶媒は分子間の相互作用を起こしやすく、粘度が高いという特徴があります。
粘度が高いと電気伝導率が下がってしまうため、下記に記載する粘度が低い鎖状のカーボネート系材料と混合したものが、現在のリチウムイオン電池用電解液として採用されてることがほとんどです。
また、プロピレンカーボネート(PC)は黒鉛負極を使用している場合、うまくSEI(固定電解質相)を形成できないことが報告されており、現在環状のカーボネート系材料のメインはエチレンカーボネート(EC)です。
溶媒中のECの成分比率はおおよそ30wt%程度でしょう。
②移動度を上げるための粘度が低い材料を入れる理由
移動度を上げるために粘度ηが低い材料を使用することはイメージしやすいでしょう。
私たちが泳ごうとする際も、ドロドロの液体中を泳ぐより、サラサラの液体中を泳ぐ方が容易に移動できそうですよね。
つまり、移動度を上げる、つまり電気伝導率を上げるために粘度が低い材料を使用します。
電池に使用される粘度が低い材料として、鎖状のカーボネート系材料、DMC(ジメチルカーボネート)、EMC(エチルメチルカーボネート)、DEC(ジエチルカーボネート)が挙げられます。
これらの材料は粘度は高いのですが、比誘電率が低い傾向にあり、比誘電率が高い環状のカーボネート系材料と混合し、使用されます。
関連記事
リチウムイオン電池の構成材料の危険物の分類
SEI(固体電解質相)とは?
エネルギー密度とは?
家庭用蓄電池設置のメリット・デメリット
電気自動車、プラウインハイブリッド車の違い
酸化、還元とは?アノード、カソードとは?
電解質の塩(LiPF6)に求められる特性
電解液の添加剤とは(VCやFEC)
電解液の溶媒に求められる特性 良質なSEIを形成すること
一般的なリチウムイオン電池では負極に黒鉛を使用することが多く、黒鉛負極を使用した場合は、
初回充電時に負極活物質表面にSEI(固体電解質相)と呼ばれる皮膜を形成します。
負極活物質の表面に形成され、電解液の分解を抑制しLiイオンのみを通す役割を持ちます。
Liイオンを通すため、このSEIの形成の仕方が悪いと、電池の内部抵抗が大きくなります。
また、SEIは電解液の分解を抑制するといっても速度論的に抑制しているだけであり、
非常にゆっくりではありますが電解液が分解し、SEIとして分解物が堆積していきます。
これが電池の劣化(容量低下、抵抗上昇)の原因の一つとなるため、良質なSEIを作ることは
内部抵抗の低減だけでなく、寿命特性の向上にもつながります。
良質なSEIを形成するために上に紹介した
・環状系カーボネート(ECやPC等)
・鎖状カーボネート(DMC、EMC、DEC等)
の他に易還元性(還元されやすい)材料であるVCやFECといった添加剤を0.X%~数%添加します。
(※他にも、引火点が低くより燃えにくいことやコストが低いことが電解液には求められます。)
関連記事
リチウムイオン電池の構成材料の危険物の分類
SEI(固体電解質相)とは?
エネルギー密度とは?
家庭用蓄電池設置のメリット・デメリット
電気自動車、プラウインハイブリッド車の違い
酸化、還元とは?アノード、カソードとは?
電解質の塩(LiPF6)に求められる特性
電解液の添加剤とは(VCやFEC)
エチレンカーボネート(EC)の物性
電解液の溶媒を構成している成分であるエチレンカーボネート(EC)は別名炭酸エチレンとも呼びます。
MSDSなどでは見づらい場合があり、ここではエチレンカーボネートの物性についてまとめましたので参考にしてください。リチウムイオン電池のおける取扱説明書に記載する場合があるCAS No(CAS番号)も記載しています。
エチレンカーボネートの分子構造
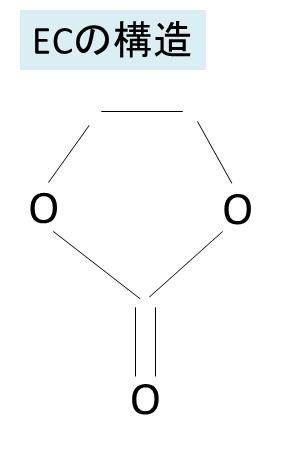
エチレンカーボネートの分子量
エチレンカーボネート(EC)の分子量は88.06 g/mol です。
エチレンカーボネートの密度
エチレンカーボネート(EC)の密度(比重)は 1.032 g/mol (20℃)です。
エチレンカーボネートの分子式
エチレンカーボネート(EC)の分子式はC3H4O3です。
エチレンカーボネートの沸点
エチレンカーボネート(EC)の沸点は244℃です。
エチレンカーボネートの引火点
エチレンカーボネート(EC)の密閉下での引火点は152℃です。
エチレンカーボネートの融点・凝固点
エチレンカーボネート(EC)の融点・凝固点は36.4℃です。
エチレンカーボネートの匂い(臭い)
意外かもしれませんがエチレンカーネート(EC)単体では、無臭です。
エチレンカーボネートの誘電率
エチレンカーボネート(EC)の誘電率εは95.3です。
エチレンカーボネートのCAS No.
エチレンカーボネート(EC)のCAS No.は 96-49-1 です。
粘度
エチレンカーボネート(EC)は常温で固体のため、粘度は測定できません。
リチウムイオン電池の電解液の溶媒の構成成分として知っておくべき特徴
エチレンカーボネート(EC)は常温で白色の固体でです。また、エチレンカーボネート(EC)単体では、危険物に該当しません。
関連記事
リチウムイオン電池の構成材料の危険物の分類
SEI(固体電解質相)とは?
エネルギー密度とは?
家庭用蓄電池設置のメリット・デメリット
電気自動車、プラウインハイブリッド車の違い
酸化、還元とは?アノード、カソードとは?
電解質の塩(LiPF6)に求められる特性
電解液の添加剤とは(VCやFEC)
ジエチルカーボネート(DEC)の物性
電解液の溶媒を構成している成分であるジエチルカーボネート(DEC)は別名炭酸ジエチルとも呼びます。
MSDSなどでは見づらい場合があり、ここではジエチルカーボネート(DEC)の物性についてまとめましたので参考にしてください。リチウムイオン電池のおける取扱説明書に記載する場合があるCAS No(CAS番号)も記載しています。
ジエチルカーボネート(DEC)の分子構造
ジエチルカーボネート(DEC)の分子量
ジエチルカーボネート(DEC)の分子量は118.13 g/mol です。
ジエチルカーボネート(DEC)の密度
ジエチルカーボネート(DEC)の密度(比重)0.97 g/mol (20℃)です。
ジエチルカーボネート(DEC)の分子式
ジエチルカーボネート(DEC)の分子式はC5H10O3です。
ジエチルカーボネート(DEC)の沸点
ジエチルカーボネート(DEC)の沸点は126.8℃です。
ジエチルカーボネート(DEC)の引火点
ジエチルカーボネート(DEC)の密閉下での引火点は32.8℃です。
ジエチルカーボネート(DEC)の融点・凝固点
ジエチルカーボネート(DEC)の融点・凝固点は-43℃です。
ジエチルカーボネート(DEC)の匂い(臭い)
ジエチルカーボネート(DEC)は甘い匂い(エステル臭)がします。
ジエチルカーボネート(DEC)の誘電率
ジエチルカーボネート(DEC)の誘電率εは2.8です。
ジエチルカーボネート(DEC)のCAS No.
ジエチルカーボネート(DEC)のCAS No.は 108-58-0 です。
ジエチルカーボネート(DEC)の粘度
ジエチルカーボネート(DEC)の粘度は21℃で0.8CPsです。。
リチウムイオン電池の電解液の溶媒の構成成分として知っておくべき特徴
ジエチルカーボネート(DEC)を入れることで、常温で固体のECと混ぜた混合物も液体になります。
低温で固体に近づくとリチウムイオン電池の内部抵抗が上昇してしまうために、DECなどの鎖状カーボネートがあることでリチウムイオン電池の低温特性を向上させています。
DEC単体では危険物第4類、第2石油類に分類されます。
関連記事
リチウムイオン電池の構成材料の危険物の分類
SEI(固体電解質相)とは?
エネルギー密度とは?
家庭用蓄電池設置のメリット・デメリット
電気自動車、プラウインハイブリッド車の違い
酸化、還元とは?アノード、カソードとは?
電解質の塩(LiPF6)に求められる特性
電解液の添加剤とは(VCやFEC)
エチルメチルカーボネート(EMC)の物性
電解液の溶媒を構成している成分であるエチルメチルカーボネート(EMC)は別名炭酸エチルメチルとも呼びます。
MSDSなどでは見づらい場合があり、ここではエチルメチルカーボネート(EMC)の物性についてまとめましたので参考にしてください。リチウムイオン電池のおける取扱説明書に記載する場合があるCAS No(CAS番号)も記載しています。
エチルメチルカーボネート(EMC)の分子構造
エチルメチルカーボネート(EMC)の分子量
エチルメチルカーボネート(EMC)の分子量は104.1 g/mol です。
エチルメチルカーボネート(EMC)の密度
エチルメチルカーボネート(EMC)の密度(比重)は1.01 g/mol (20℃)です。
エチルメチルカーボネート(EMC)の分子式
エチルメチルカーボネート(EMC)の分子式はC4H8O3です。
エチルメチルカーボネート(EMC)沸点
エチルメチルカーボネート(EMC)の沸点は109℃です。
エチルメチルカーボネート(EMC)引火点
エチルメチルカーボネート(EMC)の密閉下での引火点は23℃です。
エチルメチルカーボネート(EMC)の融点・凝固点
エチルメチルカーボネート(EMC)の融点・凝固点は-55℃です。
エチルメチルカーボネート(EMC)の匂い(臭い)
エチルメチルカーボネート(EMC)は甘い匂い(エステル臭)がします,。
エチルメチルカーボネート(EMC)の誘電率
エチルメチルカーボネート(EMC)の誘電率εは2.9です。
エチルメチルカーボネート(EMC)のCAS No.
エチルメチルカーボネート(EMC)のCAS No.は 623-53-0 です。
エチルメチルカーボネート(EMC)粘度
エチルメチルカーボネート(EMC)の粘度は0.7CPa (21℃)です。
リチウムイオン電池の電解液の溶媒の構成成分として知っておくべき特徴
エチルメチルカーボネート(EMC)は単体では、危険物に該当しません。
関連記事
リチウムイオン電池の構成材料の危険物の分類
SEI(固体電解質相)とは?
エネルギー密度とは?
家庭用蓄電池設置のメリット・デメリット
電気自動車、プラウインハイブリッド車の違い
酸化、還元とは?アノード、カソードとは?
電解質の塩(LiPF6)に求められる特性
電解液の添加剤とは(VCやFEC)
ジメチルカーボネート(DMC)の物性
電解液の溶媒を構成している成分であるジメチルカーボネート(DMC)は別名炭酸ジメチルとも呼びます。
MSDSなどでは見づらい場合があり、ここではジメチルカーボネート(DMC)の物性についてまとめましたので参考にしてください。リチウムイオン電池のおける取扱説明書に記載する場合があるCAS No(CAS番号)も記載しています。
ジメチルカーボネート(DMC)の分子構造
ジメチルカーボネート(DMC)の分子量
ジメチルカーボネート(DMC)の分子量は90.08g/mol です。
ジメチルカーボネート(DMC)の密度
ジメチルカーボネート(DMC)の密度(比重)は1.07g/mol (20℃)です。
ジメチルカーボネート(DMC)の分子式
ジメチルカーボネート(DMC)の分子式はC3H6O3です。
ジメチルカーボネート(DMC)の沸点
ジメチルカーボネート(DMC))の沸点は90.3℃です。
ジメチルカーボネート(DMC)の引火点
ジメチルカーボネート(DMC)の密閉下での引火点は17℃です。
ジメチルカーボネート(DMC)の融点・凝固点
ジメチルカーボネート(DMC)の融点・凝固点は0.5℃です。
ジメチルカーボネート(DMC)の匂い(臭い)
ジメチルカーボネート(DMC)は甘い匂い(エステル臭)がします。
ジメチルカーボネート(DMC)の誘電率
ジメチルカーボネート(DMC)の誘電率εは2.8です。
ジメチルカーボネート(DMC)のCAS No.
ジメチルカーボネート(DMC)のCAS No.は616-38-6です。
ジメチルカーボネート(DMC)の粘度
ジメチルカーボネート(DMC)の粘度は 0.6CPs (21℃)です。
リチウムイオン電池の電解液の溶媒の構成成分として知っておくべき特徴
ジメチルカーボネート(DMC)は消防法上の危険物の第4類、第1石油類に分類されます。
関連記事
リチウムイオン電池の構成材料の危険物の分類
SEI(固体電解質相)とは?
エネルギー密度とは?
家庭用蓄電池設置のメリット・デメリット
電気自動車、プラウインハイブリッド車の違い
酸化、還元とは?アノード、カソードとは?
電解質の塩(LiPF6)に求められる特性
電解液の添加剤とは(VCやFEC)
プロピレンカーボネート(PC)の物性
一般的なリチウムイオン電池には負極活物質に黒鉛を使用しますが、黒鉛使用時は電解液のメインの構成成分にPC(プロピレンカーボネート)を使用することができずに、EC(エチレンカーボネート)が使用されます。
これは、ECを使用した電解液では、電池の初回充電時に黒鉛表面にSEI被膜というものが形成され、このSEIがあることで劣化を抑制しつつもLiイオンの電導が確保されます。
一言でいいますと、PCをメインで使用した電解液では、この被膜がうまく形成されません。そのため、黒鉛を負極活物質に使用したリチウムイオン電池では、電解液にPCを使用することができません。
ただ、別の負極活物質(易黒鉛化炭素、難黒鉛化炭素)であればものによってはPCを使用できる可能性があります。
上述のような電解液の溶媒を構成している成分であるプロピレンカーボネート(PC)の物性について解説していきます。プロピレンカーボネート(PC)別名を炭酸プロピレンと呼びます。
MSDSなどでは見づらい場合があり、ここではプロピレンカーボネート(PC)の物性についてまとめましたので参考にしてください。リチウムイオン電池のおける取扱説明書に記載する場合があるCAS No(CAS番号)も記載しています。
プロピレンカーボネート(PC)の分子構造
プロピレンカーボネート(PC)の分子量
プロピレンカーボネート(PC)の分子量は102.09g/mol です。
プロピレンカーボネート(PC)の密度
プロピレンカーボネート(PC)の密度(比重)は1.205g/mol (20℃)です。
プロピレンカーボネート(PC)の分子式
プロピレンカーボネート(PC)の分子式はC4H6O3です。
プロピレンカーボネート(PC)の沸点
プロピレンカーボネート(PC)の沸点は241.7℃です。
プロピレンカーボネート(PC)の引火点
プロピレンカーボネート(PC)の密閉下での引火点は132℃です。
プロピレンカーボネート(PC))の融点・凝固点
プロピレンカーボネート(PC)の融点・凝固点は-49℃です。
プロピレンカーボネート(PC)の匂い(臭い)
プロピレンカーボネート(PC)は無臭です。
プロピレンカーボネート(PC)の誘電率
プロピレンカーボネート(PC)の誘電率εは64.4です。
プロピレンカーボネート(PC)のCAS No.
プロピレンカーボネート(PC)のCAS No.は108-32-7です。
プロピレンカーボネート(PC)の粘度
プロピレンカーボネート(PC)の粘度は 2.5CPs (21℃)です。
リチウムイオン電池の電解液の溶媒の構成成分として知っておくべき特徴
プロピレンカーボネート(PC)は消防法上の危険物の第4類、第3石油類に分類されます。
関連記事
リチウムイオン電池の構成材料の危険物の分類
SEI(固体電解質相)とは?
エネルギー密度とは?
家庭用蓄電池設置のメリット・デメリット
電気自動車、プラウインハイブリッド車の違い
酸化、還元とは?アノード、カソードとは?
電解質の塩(LiPF6)に求められる特性
電解液の添加剤とは(VCやFEC)
リチウムイオン電池の電解液(溶媒)の材料化学 関連ページ
- リチウムイオン電池の正極活物質(正極材)とコバルト酸リチウム(LiCoO2:LCO)の反応と特徴
- 【容量の算出】コバルト酸リチウムの理論容量を算出する方法
- リン酸鉄リチウム(LFP)の反応と特徴 Li-Fe(リチウムフェライト)電池とは?鉛蓄電池の置き換えに適している?
- 【容量の算出】マンガン酸リチウムの理論容量を算出する方法
- リン酸鉄リチウム(LFP)の合成方法
- 【容量の算出】リン酸鉄リチウムの理論容量を算出する方法
- マンガン酸リチウムの反応と特徴
- リチウムイオン電池における導電助剤の位置づけ VGCF(気相成長炭素)の特徴
- 正極の電極構造
- リチウムイオン電池の負極活物質(負極材) 黒鉛(グラファイト)の反応と特徴
- グラファイト(黒鉛)とグラフェンの違い【リチウムイオン電池の導電助剤】
- 難黒鉛化炭素(ハードカーボン)の反応と特徴【リチウムイオン電池の負極材(負極活物質)】
- 易黒鉛化炭素(ソフトカーボン)の反応と特徴【リチウムイオン電池の負極材(負極活物質)】
- リチウムイオン電池の負極活物質(負極材) チタン酸リチウム(LTO)の反応と特徴
- リチウムイオン電池の電解液(溶媒)に入れる添加剤の役割と種類(VC,FECなど)
- リチウムイオン電池の電解液(塩)の材料化学 なぜ市販品ではLiPF6が採用されているか?
- リチウムイオン電池におけるセパレータの位置づけと材料化学
- リチウムイオン電池におけるバインダーの位置づけと材料化学
- 溶媒和・脱溶媒和とは?ボルンの式とは?【リチウムイオン電池の反応と溶媒和・脱溶媒和)
- 【リチウムイオン電池材料の評価】セパレータの透気度とは?
- リチウムイオン電池のセパレータに求められる特性
- リチウムイオン電池の寿命予測方法(ルート則)
- リチウムイオン電池の寿命予測方法(内部抵抗の上昇の予測)
- リチウムイオン電池の劣化後の放電曲線(作動電圧)の予測方法
- 【アレニウスの式使用問題演習】リチウムイオン電池の寿命予測をExcelで行ってみよう!
- 【続アレニウスの式使用問題演習】リチウムイオン電池の寿命予測をExcelで行ってみよう!その2
- 【サイクル試験の寿命予測、劣化診断】リチウムイオン電池の寿命予測(サイクル試験)をExcelで行ってみよう!
- リチウムイオン電池の寿命予測方法 ルート則とべき乗則
- XRDの原理と解析方法・わかること X線回折装置とは?
- XRDなどに使用されるKα線・Kβ線とは?
- XPSの原理と解析方法・わかること
- ラマン分光法の原理と解析方法・わかること
- IR:赤外分光法の原理と解析方法・わかること
- ICP:誘導結合高周波プラズマ分析の原理と解析方法・わかること
- SEMの原理と解析方法・わかること
- 化学におけるinsituとはどういう意味?読み方は?
- ランベルトベールの法則と計算方法【演習問題】
- DSCの測定原理と解析方法・わかること
- ヘンリーの吸着等温式とは?導出過程は?
- ラングミュア(langmuir)の吸着等温式とは?導出過程は?
- 化学吸着と物理吸着の違いは?活性炭と物理吸着【電気二重層キャパシタ材料としても使用】
- 【演習問題】比表面積を求める方法【BET吸着_ラングミュア吸着】
- 【比表面積の計算】BET吸着とは?導出過程は?【リチウムイオン電池の解析】
- 【材料力学】弾性係数(ヤング率)とは?計算方法(求め方)と使用方法【リチウムイオン電池の構造解析】
- 【材料力学】熱ひずみ・熱応力とは?導出と計算方法は?
- 【材料力学】ポアソン比とは?求め方と使用方法【リチウムイオン電池の構造解析】
- 【材料力学】応力-ひずみ線図とは?【リチウムイオン電池の構造解析】
- 【材料力学】材料のたわみ計算方法は?断面二次モーメント使用【リチウムイオン電池の構造解析】
- 【材料力学】クリープとは 材料のクリープ
- 【材料力学】断面二次モーメントとは?断面係数とは?【リチウムイオン電池の構造解析】
- 【材料力学】剥離強度とは?電極の剥離強度【リチウムイオン電池の構造解析】
- 【材料力学】トルクと動力・回転数 導出と計算方法【演習問題】
- 【材料力学】馬力と動力の変換方法【演習問題】
- 【材料力学】公差とは?公差の計算と品質管理
- 寸法収縮・成型収縮とは?計算問題を解いてみよう【演習問題】
- 【材料力学】固体の体積膨張率(体積膨張係数)とは?固体の体積膨張率の計算を行ってみよう【演習問題】
- 【材料力学】気体の体積膨張率(体積膨張係数)とは?気体の体積膨張率の計算を行ってみよう【演習問題】
- ダイキャスト(ダイカスト)と鋳造(ちゅうぞう)の違いは?
- 絶縁距離とは?沿面距離と空間距離の違いは?
- 電池の安全性試験の種類
- 電池の安全性試験の位置づけと過充電試験
- 過充電試験の反応詳細
- リチウムイオン電池の外部短絡試験とは?
- リチウムイオン電池の内部短絡試験とは?
- リチウムイオン電池の釘刺し試験とは?
- リチウムイオン電池の振動試験とは?
- リチウムイオン電池の熱衝撃試験とは?
- リチウムイオン電池の過放電試験とは?
- 【演習問題】表面張力とは?原理と計算方法【リチウムイオン電池パックの接着】
- 接着剤が付く理由は?アンカー効果とは?【リチウムイオン電池パックの接着】
- 弾性接着剤とは?特徴は?シリコーンと変成シリコーンの違いは?【リチウムイオン電池パックの接着】
- ホットメルト系接着剤とは?特徴は?【リチウムイオン電池パックの接着】
- PPやPEは接着が難しい?理由と解決策は?【リチウムイオン電池パックの接着】
- エポキシ接着剤とは?特徴は?【リチウムイオン電池パックの接着】
- 接着と粘着、接着剤と粘着剤の違いは?
- 接着剤における1液型と2液型(1液系と2液系)の違いは?
- 【角型電池】リチウムイオン電池における安全弁(ガス排出弁)とは?
- 振動試験における対数掃引とは?直線掃引との違いは?
- 振動試験時の共振とは?【リチウムイオン電池の安全性】
- 【リチウムイオン電池の熱衝撃試験】熱膨張係数の違いによる応力の計算方法
- 【演習問題】金属の電気抵抗と温度の関係性 温度が上がると抵抗も上がる?
- 図積分とは?Excelで図積分を行ってみよう!
- 多孔度(空隙率・空間率)とは何?多孔度の計算方法は?電極の多孔度と電池性能の関係
- 正極にはなぜAl箔を使用?負極はなぜCu箔を使用?
- 真密度、見かけ密度(粒子密度)、タップ密度、嵩密度の違いは?
- 粉体における一次粒子・二次粒子とは?違いは?
- 負極のCu箔の作製方法 圧延銅箔
- 負極のCu箔の作製方法 電解銅箔
- 【リチウムイオン電池の水分測定】カールフィッシャー法の原理と測定方法
- 【演習問題】細孔径を求める方法【水銀圧入法】
- mmHgとPa,atmを変換、計算する方法【リチウムイオン電池の解析】
- 蒸着とは?CVDとPVDの違いは?
- 【次世代電池】全固体電池とは?反応や特徴、メリット、デメリットは?
- 【リチウムイオン電池の材料】シリコン系負極の反応と特徴、メリット、デメリットは?【次世代電池の材料】
- 【次世代電池】イオン液体とは?反応や特徴、メリット、デメリット(課題)は?
- プレドープ、プレドープ電池とは?リチウムイオン電池や電気二重層キャパシタとの違いは?
- 粘度と動粘度の変換(換算)方法 計算問題を解いてみよう【粘度と動粘度の違い】
- エネルギー変換効率とは?燃料電池の理論効率・理論起電力の計算方法【演習問題】
- 電位、電圧、電位差、電圧降下の違い【リチウムイオン電池関連の用語】
- SBR(スチレンブタジエンゴム)とは?ゴムにおける加硫とは?【リチウムイオン電池の材料】
- フィラーとは何か?剤と材の違いは?【リチウムイオン電池の材料】
- 有機酸とは?有機酸に対する耐性とは?【リチウムイオン電池の材料】
- 潜熱と顕熱とは?潜熱と顕熱の違いは?
- ポリオレフィンとは何か?【リチウムイオン電池の材料】
- エンプラ、スーパーエンプラとは何か?エンプラとスーパーエンプラの違いは?【リチウムイオン電池の材料】
- 化学におけるドープとは?プレドープとの違いは?
- エクセルギ-とは?エクセルギ-の計算問題【演習問題】
- エマルジョン・ラテックスとは?ラテックス系バインダーとは?【リチウムイオン電池の材料】
- 電池におけるプラトーの意味は?【リチウムイオン電池の用語】
- 単位のrpmとは?rpmの変換・計算方法【演習問題】
- 平均自由行程とは?式と導出方法は?【演習問題】
- 弾性衝突と非弾性衝突の違いは?【演習問題】
- アルキメデスの原理と浮力 浮力の計算問題を解いてみよう【演習問題】
- シーリングとコーキングの違いは?
- 固体高分子形燃料電池(PEFC)における電解質膜の役割は?種類は?
- 固体高分子形燃料電池(PEFC)における電極触媒とは?役割や種類は?
- 固体高分子形燃料電池(PEFC)における酸素還元活性(ORR)とは?
- 固体高分子形燃料電池(PEFC)におけるECSA(白金有効利用面積)とは?
- 固体高分子形燃料電池(PEFC)におけるフラッディング・ドライアウトとは?
- 固体高分子形燃料電池(PEFC)におけるクロスオーバー(ガスクロスオーバー)とは?
- 固体高分子形燃料電池(PEFC)におけるアイオノマー(イオノマー)とは?役割は?
- wt%(重量パーセント)・mass(質量パーセント)とは?計算方法は?【演習問題】
- 放射能の半減期 計算方法と導出方法は?【反応速度論】
- ストークス半径とイオン半径
- ファントホッフの式とは?導出と計算方法は【平衡定数の温度依存性】
- 化学的安定性 HOMO-LUMO
- 遠心分離と遠心効果 計算と導出方法【演習問題】
- rpmをGに変換する方法 計算問題を解いてみよう【演習問題】
- w/w%・w/v%・v/v% 定義と計算方法【演習問題】
- 分子式・組成式・化学式 見分け方と違いは?【演習問題】
- テルミット反応 リチウムイオン正極材のリサイクル
- 誘電率と比誘電率 換算方法【演習問題】
- 誘電体(絶縁体)と誘電分極(イオン分極・電子分極・配向分極)
- 導体と静電誘導 静電誘導と誘電分極との違いは?
- 屈折率と比誘電率の関係 計算問題を解いてみよう【演習問題】
- 双極子と双極子モーメント 意味と計算方法
- 回折格子における格子定数とは?格子定数の求め方
- 引火点と発火点(着火点)の違いは?【危険物取扱者乙4・甲種などの考え方】
- 燃焼範囲とは【危険物取扱者乙4・甲種などの考え方】
- 危険物における自然発火とは【危険物取扱者乙4・甲種などの考え方】
- 危険物における指定数量 指定数量と倍数の計算方法【危険物取扱者乙4・甲種などの考え方】
- 危険物における保安距離や保有空地とは【危険物取扱者乙4・甲種などの考え方】
- 光速と音速はどっちが早いのか 光速と音速のマッハ数は?雷におけるの光と音の関係は?
- マッハ数の定義は?計算問題を解いてみよう【演習問題】
- 1光年の意味とその距離は 地球何周分?ロケットでは何年かかる?新幹線では?
- アンモニアの分子の形(立体構造)が三角錐(四面体)になる理由は?三角錐と正四面体の違いは?アンモニアの結合角は107度?
- 水分子(H2O)の形が直線型ではなく折れ線型となる理由 水分子の形が直線型ではなく折れ線型となる理由 水の結合角が104.5度となる理由
- 二酸化炭素(CO2)の形が折れ線型ではなく直線型である理由
- メタン(CH4)の形が正四面体である理由 結合角は109.5度(°)?
- 二硫化炭素(CS2)の形が折れ線型ではなく直線型となる理由 二硫化炭素の結合角が180度となる理由
- 結合角の意味 代表的な結合角の種類
- 【材料力学】安全率の定義とその計算方法 基準応力・許容応力との関係
- 非極性と無極性の違い
- 共有電子対と非共有電子対の見分け方、数え方
- 極性と無極性の違い 極性分子と無極性分子の見分け方
- 非共有電子対と不対電子の定義と違い
- バスバーの許容電流の定義と計算方法
- 抵抗値と抵抗率(体積抵抗率)の定義と違い
- リチウムイオン電池の正極の組成
- 【次世代電池】ナトリウムイオン電池(ソディウムイオン電池)とは?反応や特徴、メリット、デメリットは?
- リチウムイオン電池で使用される絶縁体
- リチウムイオン電池のおける増粘剤(CMC)の役割
- 古いリチウムイオン電池を使用しても大丈夫なのか
- 二酸化炭素(CO2)の化学式・分子式・構造式・電子式・イオン式・分子量は?イオン反応式は?
- アンモニアの化学式・分子式・構造式・電子式・イオン式・分子量は?イオン反応式は?
- 水(H2O)の化学式・分子式・構造式・電子式・イオン式・分子量は?代表的な反応式は?
- メタンの化学式・分子式・構造式・電子式・イオン式・分子量は?イオン反応式は?
- エタンの化学式・分子式・構造式・電子式・分子量は?代表的な反応式は?エタンの完全燃焼の反応
- プロパンの化学式・分子式・構造式・電子式・分子量は?プロパンの代表的な反応式は?プロパンの完全燃焼の反応
- 硫化水素(H2S)の化学式・分子式・構造式・電子式・分子量は?硫化水素の代表的な反応式は?
- 二硫化炭素(CS2)の化学式・分子式・構造式・電子式・分子量は?二硫化炭素の代表的な反応式は?
- 酸素(O2)の化学式・分子式・構造式・電子式・分子量は?酸素の代表的な反応式は?
- 塩素(Cl2)の化学式・分子式・構造式・電子式・分子量は?塩素の代表的な反応式は?
- ヨウ素(l2)の化学式・分子式・構造式・電子式・分子量は?ヨウ素の代表的な反応式は?
- 窒素(N2)の化学式・分子式・構造式・電子式・分子量は?窒素の代表的な反応式は?
- 硫酸の化学式・分子式・構造式・電子式・分子量は?硫酸の代表的な反応式は?
- 塩酸(塩化水素:HCl)の化学式・分子式・構造式・電子式・分子量は?塩酸の電気分解やアルミニウムとの反応式は?塩化水素と塩酸の違い
- 硝酸の化学式・分子式・構造式・電子式・イオン式・分子量は?硝酸の工業的製法のオストワルト法の反応式は?濃硝酸と銅との反応・希硝酸と銅との反応式は?
- フッ酸(フッ化水素:HF)の化学式・分子式・構造式・電子式・分子量は?塩化水素とフッ酸の違い
- 酢酸の化学式・分子式・構造式・電子式・イオン式・分子量は?酢酸の電離の反応式は?
- 水が氷になると体積が増加する理由 水と氷の体積比は?【膨らむのはなぜ?】
- 水が水蒸気になると体積は何倍になるのか?体積比の計算方法
- 導電率と抵抗率の換算(計算)方法
- 単位のジーメンス(S)の意味 ジーメンスを計算(換算)してみよう
- コンダクタンスと電気抵抗 コンダクタンスの計算方法(求め方)【演習問題】
- ヘンリーの法則とは?計算問題を解いてみよう
- 水素結合とは?分子間力との関係 水素結合の強さは?水素結合が起こる物質は?沸点も上がりやすいのか?水素結合と方向性
- 電気陰性度とは?電気陰性度の大きさと周期表との関係 希ガスと電気陰性度との関係
- 電流積算値と積算電流 計算問題を解いてみよう【演習問題】
- Wh(ワットアワー:ワット時定格量)とJ(ジュール)の変換方法 計算問題を解いてみよう
- C(クーロン)・電圧V(ボルト)・J(ジュール)の変換(換算)方法 計算問題を解いてみよう
- 共役酸と共役塩基とは?
- C(クーロン)・電流A(アンペア)・時間s(秒)の変換(換算)方法 計算問題を解いてみよう
- C(クーロン)・eV(電子ボルト:エレクトロンボルト)の変換(換算)方法 計算問題を解いてみよう
- エネルギーの単位J(ジュール)とeV(電子ボルト:エレクトロンボルト)の変換(換算)方法 計算問題を解いてみよう
- eV(電子ボルト:エレクトロンボルト)と速度vの変換(換算)方法 計算問題を解いてみよう
- g(グラム)とml(ミリリットル)の変換(換算)方法 計算問題を解いてみよう
- J(ジュール)とW(ワット)の変換(換算)方法 計算問題を解いてみよう
- J(ジュール)とcal(カロリー)の換算(変換)方法 計算問題を解いてみよう
- 荷重の単位N(ニュートン)と応力の単位Pa(パスカル)の変換方法 計算問題を解いてみよう
- 昇華性物質の代表例は?融点はどのくらい?状態図との関係は?
- シアン化水素(HCN)の化学式・分子式・構造式・電子式・分子量は?シアン化水素の分子の形や極性は?製造時の反応(工業的製法)
- W(ワット)とV(ボルト)とA(アンペア)の変換(換算)方法 計算問題を解いてみよう【1aは何ワット、1aは何ボルト】
- MPa(メガパスカル)とN/mm2の変換(換算)方法 計算問題を解いてみよう
- せん断応力とは?せん断応力の計算問題を解いてみよう
- Pa(パスカル)をkg、m、s(秒)を使用して表す方法
- ppmを濃度mg/Lに変換(換算)する方法 計算問題を解いてみよう【演習問題】
- MPa(メガパスカル)とN/cm2の変換(換算)方法 計算問題を解いてみよう
- MPa(メガパスカル)とN/m2の変換(換算)方法 計算問題を解いてみよう
- MPa(メガパスカル)とN/mは変換できるのか
- ppmをmg/Kgに変換(換算)する方法 計算問題を解いてみよう【演習問題】
- メタノール(CH3OH)の化学式・分子式・構造式・電子式・示性式・イオン式・分子量は?硝酸の工業的製法のオストワルト法の反応式は?代表的な反応式は?
- エタノール(C2H5OH)の化学式・分子式・構造式・電子式・示性式・イオン式・分子量は?代表的な反応式は?
- 分子内脱水と分子間脱水の違いは?
- kN(キロニュートン)とkg(キログラム)は換算できるのか?knとkgfの計算問題を解いてみよう
- ppmとppbの変換(換算)方法 計算問題を解いてみよう【演習問題】
- ppmをμg/gに変換(換算)する方法 計算問題を解いてみよう【演習問題】
- メタノール(CH3OH)の毒性は?エタノール(C2H5OH)なぜお酒なのか?は
- アルコールランプの燃料の主成分がエタノールでなくメタノールな理由
- エチレン(C2H4)の化学式・分子式・構造式・電子式・示性式・分子量は?代表的な反応式は?
- アセチレン(C2H2)の分子式・構造式・電子式・示性式・分子量は?アセチレン(C2H2)の完全燃焼の反応式は?
- 水の蒸発熱(気化熱:蒸発エンタルピー)の計算問題を解いてみよう【蒸発熱と温度変化】
- アセトン(C3H6O)の化学式・分子式・構造式・電子式・示性式・分子量は?平面上にあり、分子の極性がある理由は?アセトンの代表的な用途は?
- トルエン(C7H8)の化学式・分子式・構造式・電子式・示性式・分子量は?トルエンの代表的な用途は?
- キシレン(C8H10)の化学式・分子式・構造式・電子式・示性式・分子量は?キシレンの代表的な用途は?
- 【材料力学】引張応力と引張荷重(強度)の関係は?引張応力の計算問題を解いてみよう【求め方】
- 【材料力学】圧縮応力と圧縮荷重(強度)の関係は?圧縮応力の計算問題を解いてみよう【求め方】
- 化学におけるNMPとは?NMPの分子式・構造式・電子式・示性式・分子量は?NMPと危険物 NMPの沸点は?
- 化学におけるアミンとは?なぜアミンは塩基性なのか?1級・2級・3級アミンの見分け方
- エチレングリコールの化学式・分子式・示性式・構造式・電子式・イオン式・分子量は?反応式は?工業的製法は?
- フマル酸・マレイン酸・フタル酸の違いと見分け方(覚え方)
- ギ酸(蟻酸)の化学式・分子式・構造式・電子式・イオン式・分子量は?
- シュウ酸(C2H2O4)の化学式・分子式・構造式・電子式・イオン式・分子量は?
- 空気比(空気過剰係数:記号m)と理論空気量や酸素濃度との関係 最適な空気比mの計算し、省エネしよう【演習問題】
- 圧力計と連成計と真空計の違い 測定範囲や使用用途(使い分け)は?
- MPa(メガパスカル)とKPa(キロパスカル)の変換(換算)方法 計算問題を解いてみよう
- オクタン価とセタン価とは? 計算問題を解いてみよう【演習問題】
- カルボン酸では分子内脱水が起こるのか?マレイン酸・フタル酸などのカルボン酸の脱水反応式
- 乳酸(C3H6O3)の分子式・構造式・示性式・電子式・分子量は?
- アミノ酸とは?アルミの酸と鏡像異性体(光学異性体) D体L体とは?アミノ酸とタンパク質の関係(ペプチド結合とは?)
- 不斉炭素原子とは? 鏡像異性体・旋光性・キラリティーとの関係 RS表記法とDL表記法とは?
- ラセミ体とメソ体の違いと見分け方
- キラルとアキラルの違いは?
- ヒドロキシ酸とは?
- 親水性と疎水性の違い
- ゾルとゲルの違いは?
- エナンチオマーとジアステレオマーの違いは?
- フィッシャー投影図とニューマン投影図
- 立体配置と立体配座
- アルコールとカルボン酸の脱水によりエステルを生成する反応式 エステル化と加水分解
- 5員環とは何か?5員環を持つ物質の例【リチウムイオン電池構成部材であるNMPやγブチロラクトン】
- ラクトンの定義と合成方法
- 多価アルコール(ポリオール)とは?
- グリセリン(グリセロール)の化学式・分子式・示性式・構造式・電子式・イオン式・分子量は?反応式は?工業的製法は?
- イミド・ポリイミド・イミド結合とは?リチウムイオン電池におけるポリイミド
- アミド・ポリアミド・アミド結合とは?リチウムイオン電池におけるポリアミド
- 次亜塩素酸・亜塩素酸・塩素酸・過塩素酸(Clを含むオキソ酸)の分子式(化学式)・構造式は?酸の強弱は?
- 硫酸・希硫酸・濃硫酸・熱濃硫酸の性質 共通点と違いは?
- 硫酸・亜硫酸の違いは?
- 硝酸・亜硝酸の違いは?
- グリコールとグリセリンの違いは?
- 炭酸の化学式・分子式・構造式・電子式・イオン式・分子量は?炭酸の代表的な反応式は?
- 分子間脱水と縮合の違いは?
- ε(イプシロン)カプロラクタムの分子式・示性式・電子式・構造式は?
- チオ硫酸ナトリウムの分子式・構造式・電子式・分子量は?チオ硫酸ナトリウムの代表的な反応式は?
- 66ナイロンの構造式や反応式は?ヘキサメチレンジアミンと化学式(分子式・示性式・構造式)・分子量は?
- アジピン酸の化学式(分子式・示性式・構造式)・分子量は?66ナイロンの構造式や反応式は?
- テレフタル酸の構造式・分子式・示性式・分子量は?分子内脱水して無水フタル酸になるのか?
- フタル酸の分子内脱水反応と酸無水物の無水フタル酸の構造式
- PET(ポリエチレンテレフタラート)の構造式と反応式(テレフタル酸とエチレングリコールの反応)
- 電離とは?電解質と非電解質の違いは?電気を通すか通さないか
- 電離度とは?強酸と弱酸の違いと見分け方
- 電離度とは?強塩基と弱塩基の違いと見分け方
- 水酸化ナトリウム(NaOH)の性質と用途は?
- 酸塩基におけるイオンの価数と求め方 価数の一覧付き
- 1級アルコールをからアルデヒドを経てカルボン酸まで酸化する反応 2級アルコールをケトンまで酸化する反応式
- アルコールの脱水反応(分子間脱水と分子内脱水)
- ザイツェフ則とアルコールの脱水
- 二酸化窒素(NO2)の化学式・分子式・構造式・電子式・イオン式・分子量は?二酸化窒素と水との反応式は?
- 二酸化ケイ素(SiO2)の化学式・分子式・構造式・電子式・イオン式・分子量は?イオン反応式は?(コピー)
- 一酸化炭素(CO)の化学式・分子式・構造式・電子式・イオン式・分子量は?炭素の不完全燃焼の反応式は?
- 二酸化硫黄(SO2)の化学式・分子式・構造式・電子式・分子量は?二酸化硫黄の代表的な反応式は?
- 一酸化窒素(NO)の化学式・分子式・構造式・電子式・イオン式・分子量は?一酸化窒素と水との反応式は?
- 塩化アンモンニウム(NH4Cl)の化学式・分子式・構造式・電子式・電離式・分子量は?塩素とアンモニアの混合で白煙を生じる反応式
- 水素(H2)の化学式・分子式・構造式・電子式・分子量は?水素の燃焼反応(水の生成)の反応式は?
- 過酸化水素(H2O2)の化学式・分子式・構造式・電子式・分子量は?過酸化水素の分解の反応式は?
- フッ素(F2)の化学式・分子式・構造式・電子式・分子量は?フッ素の水との反応式は?
- 臭素(Br2)の化学式・分子式・構造式・電子式・分子量は?臭素の水との反応式は?
- 酸化カルシウム(CaO)の化学式・組成式・構造式・電子式・分子量は?酸化カルシウムの水との反応式は?
- オゾン(O3)の化学式・分子式・構造式・電子式・分子量は?オゾン(O3)の代表的な反応式は?
- 水酸化カルシウム(Ca(OH)2)の化学式・組成式・構造式・電子式・分子量は?水酸化カルシウム(石灰水)と二酸化炭素との反応式は?
- 炭酸カルシウム(CaCO3)の化学式・組成式・構造式・電子式・分子量は?
- アニリンの化学式・組成式・構造式・電子式・分子量は?ベンゼンからニトロベンゼンを経由しアニリンを合成する反応式は?
- 酢酸の脱水により無水酢酸を生成する反応式(分子間脱水)
- MPa(メガパスカル)とKg/cm2の変換(換算)方法 計算問題を解いてみよう
- 二酸化硫黄(SO2)の形が直線型ではなく折れ線型となる理由
- アセトアルデヒド(C2H4O)の化学式・分子式・構造式・電子式・示性式・分子量は?エタノールを酸化し、アセトアルデヒドのなる反応
- ホルムアルデヒド(CH2O)の化学式・分子式・構造式・電子式・示性式・分子量は?ホルムアルデヒドの代表的な用途は?
- 塩化ナトリウム(NaCl)の化学式・分子式・構造式・電子式・イオン式・分子量は?塩化ナトリウムと硝酸銀の反応式
- 炭酸ナトリウム(Na2CO3)の化学式・分子式・構造式・電子式・イオン式・分子量は?炭酸ナトリウムの工業的製法
- 酢酸エチル(C4H8O2)の化学式・分子式・構造式・電子式・示性式・分子量は?酢酸とエタノールから酢酸エチルを生成する反応式
- 炭酸水素ナトリウム(NaHCO3)の化学式・分子式・構造式・電子式・イオン式・分子量は?炭酸ナトリウムの工業的製法
- 【Excel】mとcmの変換(換算)方法 計算問題を解いてみよう
- m(メートル)とmm(ミリメートル)の換算(変換)方法 計算問題を解いてみよう
- m(メートル)とkm(キロメートル)の変換(換算)方法 計算問題を解いてみよう
- m(メートル)とμm(マイクロメートル)の変換(換算)方法 計算問題を解いてみよう
- gとmgの変換(換算)方法 計算問題を解いてみよう
- gとkgの変換(換算)方法 計算問題を解いてみよう
- 【Excel】エクセルを用いて休憩時間を引いた勤務時間(実働時間)を計算する方法【演習問題】
- km/hとm/sの変換(換算)方法 計算問題を解いてみよう
- アルミ缶や10円玉や乾電池などで磁石にくっつくのはどれか?
- 水の質量と体積を変換(換算)する方法 計算問題を解いてみよう【水の重さの求め方】
- 【SPI】異なる濃度の食塩水を混ぜる問題の計算方法【濃度算】
- 【SPI】食塩水を蒸発させたときの濃度の計算方法【濃度算】
- 【SPI】食塩水に水を追加したときの濃度の計算方法【濃度算】
- 水の凝固熱(凝固エンタルピー)の計算問題を解いてみよう【凝固熱と温度変化】
- 閉回路と開回路の違いは?
- カウンターアニオン:対アニオンとカウンターカチオン:対カチオンとは?
- イオン対と対イオンの違いは?
- リチウムイオン・ナトリウムイオンと同じ電子配置は?
- アルミニウムイオン・塩化物イオンと同じ電子配置は?
- 二量体と会合の違いとは?酢酸などのカルボン酸の二量体の構造式
- 黒鉛などの物質では昇華熱は結合エネルギーに相当する
- 同じ電子配置では原子番号が増えるほどイオン半径が小さくなるメカニズム
- 価電子とは?数え方や覚え方 最外殻電子との違いは?
- L(リットル)とm3(立方メートル)の変換(換算)方法 計算問題を解いてみよう
- 空気に含まれる酸素・窒素・二酸化炭素・水蒸気の割合は?円グラフで表してみよう
- 電子殻のKMLN殻とは?各々の最大数・収容数は?最外殻電子数の公式は?
- 表面積・断面積と面積の違い
- 長方形(四角)、円、配管の断面積を求める方法【直径や外径から計算】表面積・断面積と面積の違い(コピー)
- L(リットル)とcm3(立方センチメートル)の変換(換算)方法 計算問題を解いてみよう
- 希ガスの価電子の数が0であり、最外殻電子の数と違う理由
- 燃料タンクなどの円筒型タンクや角タンクの容量の計算方法
- 欠けた円(欠円)や弓形の面積の計算方法
- L(リットル)とmm3(立方ミリメートル)の変換(換算)方法 計算問題を解いてみよう
- 価標・原子価・価電子の違いは?
- ナトリウムやカリウムなどのアルカリ金属を石油や灯油中に保存する理由【リチウムは?】
- 危険物における第三類に分類される禁水性物質とは?
- mL(リットル)とccの変換(換算)方法 計算問題を解いてみよう
- メタン・エタン・プロパンの燃焼熱を計算してみよう【炭化水素の燃焼熱】
- メタノール、エタノールの燃焼熱の計算問題をといてみよう【アルコールの燃焼熱】
- 水素や酸素などの単体の生成熱は0なのか?この理由は?
- 単位のリューベ(立米)とリットル(L)の変換(換算)方法 計算問題を解いてみよう
- 水道水、ミネラルウォーター、純水、超純水、塩水などは電気を通すのか?通さないのか?その理由は?
- アルコールとエーテルの沸点の違い 水素結合が影響しているのか?
- エチレン、アセチレンの燃焼熱の計算問題をといてみよう
- 水のリューベ(立米)とトン(t)の換算(変換)方法 計算問題を解いてみよう
- J(ジュール)とkJ(キロジュール)の換算(変換)方法 計算問題を解いてみよう
- J(ジュール)とMJ(メガジュール)の換算(変換)方法 計算問題を解いてみよう
- kJ(キロジュール)とkcal(キロカロリー)の換算(変換)方法 計算問題を解いてみよう
- kJ(キロジュール)とeV(電子ボルト:エレクトロンボルト)の換算(変換)方法 計算問題を解いてみよう
- kJ(キロジュール)とMJ(メガジュール)の換算(変換)方法 計算問題を解いてみよう
- Å(オングストローム)とnm(ナノメートル)の換算(変換)方法 計算問題を解いてみよう
- μm(マイクロメートル)とnm(ナノメートル)の変換(換算)方法 計算問題を解いてみよう
- cm(センチメートル)とnm(ナノメートル)の変換(換算)方法 計算問題を解いてみよう
- mm(ミリメートル)とnm(ナノメートル)の変換(換算)方法 計算問題を解いてみよう(コピー)
- m(メートル)とnm(ナノメートル)の変換(換算)方法 計算問題を解いてみよう(コピー)(コピー)
- A(アンペア)とmA(ミリアンペア)の変換(換算)方法 計算問題を解いてみよう【1aは何maなのか】
- A(アンペア)とμA(マイクロアンペア)の変換(換算)方法 計算問題を解いてみよう
- mA(ミリアンペア)とμA(マイクロアンペア)の変換(換算)方法 計算問題を解いてみよう
- V(ボルト)とmV(ミリボルト)の変換(換算)方法 計算問題を解いてみよう
- V(ボルト)とkV(キロボルト)の変換(換算)方法 計算問題を解いてみよう
- W(ワット)とkW(キロワット)の変換(換算)方法 計算問題を解いてみよう
- W(ワット)とMW(メガワット)の変換(換算)方法 計算問題を解いてみよう
- kW(キロワット)とMW(メガワット)の変換(換算)方法 計算問題を解いてみよう
- MJ(メガジュール)とkcal(キロカロリー)の換算(変換)方法 計算問題を解いてみよう
- MJ(メガジュール)とkWh(キロワットアワー)の換算(変換)方法 計算問題を解いてみよう
- t(トン)とkg(キログラム)の変換(換算)方法 計算問題を解いてみよう
- t(トン)とg(グラム)の変換(換算)方法 計算問題を解いてみよう
- J(ジュール)とkWh(キロワットアワー)の換算(変換)方法 計算問題を解いてみよう
- kJ(キロジュール)とkWh(キロワットアワー)の換算(変換)方法 計算問題を解いてみよう
- ベンゼン(C6H6)の化学式・分子式・構造式・電子式・示性式・分子量は?ベンゼンの代表的な反応は?
- KPa(キロパスカル)とmmhgの変換(換算)方法 計算問題を解いてみよう
- 多孔質とは?ポーラスとは?マイクロポーラスとメソポーラス
- 酸素や水素などの気体の密度と比重を求める方法【空気の密度が基準】
- 窒素やアルゴンなどの気体の密度と比重を求める方法 計算問題を解いてみよう
- 気体の状態方程式における圧力・体積・気体定数・温度の単位 計算問題をといてみよう
- ニトログリセリン(C3H5N3O9)の化学式・分子式・構造式・電子式・示性式・分子量は?ニトログリセリンの代表的な化学反応式は?
- 水は100度以上にはなるのか?圧力を加えると200度のお湯になるのか?
- 富士山などの高山で水の沸点は下がる【山の気圧でお湯を沸かしたときの温度】
- 燃焼と酸化の違いは?
- 赤外線と紫外線の違いや用途は?
- 赤外線と遠赤外線、近赤外線、中赤外線の違いや用途は?
- カイロの中身は危険なのか?
- 鉄が燃焼し酸化鉄となるときの燃焼熱の計算問題をといてみよう【金属の燃焼熱】
- 銀鏡反応の原理と化学反応式 アルデヒドの検出反応
- 一酸化二窒素(N2O)の化学式・分子式・構造式・電子式・イオン式・分子量は?
- 塩素(Cl2)の性質 色、におい、密度・比重(空気より重いのか)、水に溶けると何性になるのか?
- フッ素(F2)の性質 色、におい、密度・比重(空気より重いのか)、水に溶けると何性になるのか?
- 臭素(Br2)の性質 色、におい、密度・比重(空気より重いのか)、水に溶けると何性になるのか?
- エチレンやアセチレンなどの気体の密度と比重を求める方法【空気の密度が基準】
- 硫化水素(H2S)や二酸化硫黄(SO2)などの気体の密度と比重を求める方法【空気の密度が基準】
- 二酸化炭素(CO2)や一酸化炭素(CO)などの気体の密度と比重を求める方法【空気の密度が基準】
- アルミニウムが錆びにくい理由は?【酸化被膜(アルミナ)との関係性】
- ステンレスが錆びにくい理由は?【酸化被膜、水酸化被膜との関係性】
- 気体の密度と圧力・温度との関係式は?
- 使い捨てカイロを水につけるとどうなるのか?危険なのか?【カイロの水没】
- アルミニウムにおけるアルマイト処理(陽極酸化処理)の原理と特徴
- チタンが錆びにくい理由は?【酸化被膜(二酸化チタン)との関係性】
- 冷たい空気は下に行き、温かい空気は上に行くのか【エアコンの風向の調整】
- カイロを途中で捨てたり、置きっぱなしにすると発火する危険はあるのか
- Ω(オーム)とkΩ(キロオーム)の換算(変換)方法 計算問題を解いてみよう【1キロオームは何オーム】
- Ω(オーム)とmΩ(ミリオーム)の換算(変換)方法 計算問題を解いてみよう
- Ω(オーム)とMΩ(メガオーム)の変換(変換)方法 計算問題を解いてみよう(コピー)
- kΩ(キロオーム)とMΩ(メガオーム)の変換(変換)方法 計算問題を解いてみよう
- kΩ(キロオーム)とmΩ(ミリオーム)の換算(変換)方法 計算問題を解いてみよう
- Ω(オーム)・ボルト(V)・アンペア(A)の換算(変換)方法 計算問題を解いてみよう
- 氷が水に浮く(沈む)理由は? 氷と水の密度と水素結合
- 電子供与性(ドナー性)と電子受容性(アクセプター性)とは?
- m2(平方メートル)とcm2(平方センチメートル)の換算(変換)方法 計算問題を解いてみよう
- m2(平方メートル)とmm2(平方ミリメートル)の換算(変換)方法 計算問題を解いてみよう
- m2(平方メートル)とkm2(平方キロメートル)の換算(変換)方法 計算問題を解いてみよう
- cm2(平方センチメートル)とmm2(平方ミリメートル)の換算(変換)方法 計算問題を解いてみよう
- 平米(m2)と坪の換算(変換)方法 計算問題を解いてみよう
- μm2(平方マイクロメートル)とmm2(平方ミリメートル)の換算(変換)方法 計算問題を解いてみよう
- m3(立方メートル)とmm3(立方ミリメートル)の換算(変換)方法 計算問題を解いてみよう
- m3(立方メートル)とcm3(立方センチメートル)の換算(変換)方法 計算問題を解いてみよう
- mm3(立方ミリメートル)とcm3(立方センチメートル)の換算(変換)方法 計算問題を解いてみよう
- m3(立方メートル)とkm3(立方キロメートル)の換算(変換)方法 計算問題を解いてみよう
- ha(ヘクタール)とkm2(平方キロメートル)の換算(変換)方法 計算問題を解いてみよう
- m2(平米)とm3(立米)は換算(変換)方法 計算問題を解いてみよう
- mile(マイル)とkm(キロメートル)の変換(換算方法) 計算問題を解いてみよう
- ha(ヘクタール)とm2(平方メートル)の換算(変換)方法 計算問題を解いてみよう
- N/mm2とkN/m2の換算(変換)の計算問題を解いてみよう
- n(ニュートン)とkN(キロニュートン)の換算(変換)の計算問題を解いてみよう
- N(ニュートン)とMN(メガニュートン)の換算(変換)の計算問題を解いてみよう
- kN(キロニュートン)とMN(メガニュートン)の換算(変換)の計算問題を解いてみよう
- N/mm2とkN/cm2の換算(変換)の計算問題を解いてみよう
- kgf/cm2とkN/cm2の換算(変換)の計算問題を解いてみよう
- MPa(メガパスカル)とkN/m2の変換(換算)方法 計算問題を解いてみよう(コピー)
- g/Lとkg/m3の変換(換算)方法 計算問題を解いてみよう
- cm4とmm4の変換(換算)の計算問題を解いてみよう
- cm4とm4の変換(換算)の計算問題を解いてみよう
- kPa(キロパスカル)とkg/cm2の変換(換算)方法 計算問題を解いてみよう
- kPa(キロパスカル)とpsiの変換(換算)方法 計算問題を解いてみよう
- MPa(メガパスカル)とpsiの変換(換算)方法 計算問題を解いてみよう
- kPa(キロパスカル)とbarの変換(換算)方法 計算問題を解いてみよう
- MPa(メガパスカル)とbar(バール)の変換(換算)方法 計算問題を解いてみよう
- psiとbar(バール)の変換(換算)方法 計算問題を解いてみよう
- kg/m3とg/cm3の変換(換算)方法 計算問題を解いてみよう
- kg/Lとg/cm3の変換(換算)方法 計算問題を解いてみよう
- g/cm3とg/mm3の変換(換算)方法 計算問題を解いてみよう
- g/cm3とkg/mm3の変換(換算)方法 計算問題を解いてみよう
- g/cm3とg/m3の変換(換算)方法 計算問題を解いてみよう
- 連続で外す確率の計算方法【50%の当たりで5回連続で外れる確率】
- 高位発熱量と低位発熱量の違いと変換(換算)方法【計算問題】
- 絶対湿度と相対湿度とは?乾燥空気(乾き空気)と湿潤空気(湿り空気)の違いは?
- スカラー量とベクトル量の違いは?計算問題を解いてみよう
- ベクトルの大きさの計算方法【二次元・三次元】
- 絶対座標と相対座標の定義と違いは?
- 導線の抵抗を計算する方法【断面積や長さと金属の線の抵抗】
- 等温変化でpv=一定となる理由
- 表面抵抗(シート抵抗)と体積抵抗の変換(換算)の計算を行ってみよう【表面抵抗率と体積抵抗率の違い】
- 化学における定量分析と定性分析の違いは?
- 分圧と分流とは?計算問題を解いてみよう【直列・並列と分圧・分流(分圧回路の考え方)】
- Pa・s(パスカル秒)とP(ポアズ)の換算(変換)方法 計算問題を解いてみよう
- Pa・s(パスカル秒)とcP(センチポアズ)の換算(変換)方法 計算問題を解いてみよう
- mPa・s(ミリパスカル秒)とcP(センチポアズ)の換算(変換)方法 計算問題を解いてみよう(コピー)
- mPa・s(ミリパスカル秒)とP(ポアズ)の換算(変換)方法 計算問題を解いてみよう
- 座屈荷重と座屈応力の計算問題を解いてみよう【座屈とは何か】
- 断熱変化におけるVTグラフはどのようになるのか【v-tグラフ】
- P(ポアズ)とcP(センチポアズ)の換算(変換)方法 計算問題を解いてみよう
- mPa・s(ミリパスカル秒)とPa・s(パスカル秒)の換算(変換)方法 計算問題を解いてみよう
- 単原子分子、二原子分子、多原子分子の違いは?
- 全圧と分圧とは?ドルトンの法則(分圧の法則)とは?計算問題を解いてみよう【モル分率や質量分率との関係】
- 質量分率とモル分率の変換(換算)方法【計算】
- 質量分率と体積分率の変換(換算)方法【計算】
- 質量パーセントとモル分率の変換(換算)方法【計算】
- モル濃度とモル分率の変換(換算)の計算問題を解いてみよう
- モル濃度と質量モル濃度の変換(換算)の計算問題を解いてみよう
- 分圧比とモル比(物質量比)が一致する理由【定積・定温下】
- 体積比(容積比)とモル比(物質量比)が一致する理由【定積・定温下】
- 質量比(重量比)とモル比(物質量比)・モル質量の変換(換算)の計算問題を解いてみよう【混合気体】
- 質量比(重量比)と体積比(容積比)の変換(換算)の計算問題を解いてみよう【混合気体】
- 比体積と密度の変換(換算)の計算問題を解いてみよう【比体積とは?】
- 状態方程式から空気の比体積を計算してみよう
- グレアムの法則とは?計算問題を解いてみよう【気体の拡散の公式】
- 熱変形量(熱膨張量、熱収縮量)の計算を行ってみよう【熱変形量の求め方】
- 分子速度の求め方や温度との関係性【分子速度の計算】
- 比重量とは何か?密度、比重との違い【重力加速度との関係性】
- 気体の膨張・収縮と温度との関係 計算問題を解いてみよう【シャルルの法則】
- 二乗平均速度と根二乗平均速度の公式と計算方法
- 質点の重心を求める方法【2質点系の計算】
- 電荷と電荷密度 面電荷密度(面積電荷密度)の計算方法【変換(換算)】
- 体積電荷密度(体電荷密度)・線電荷密度の計算方法【変換(換算)】
- 面密度と体積密度と線密度の変換(換算)方法 計算問題を解いてみよう
- ミリ秒(ms)と秒(s)の変換(換算)の計算問題を解いてみよう【1秒は何ミリ秒】
- ミリ秒(ms)と分(min)の変換(換算)の計算問題を解いてみよう【1分は何ミリ秒】
- ミリ秒(ms)とマイクロ秒(μs)の変換(換算)の計算問題を解いてみよう【1ミリ秒は何マイクロ秒】
- ミリ秒(ms)とナノ秒(ns)の変換(換算)の計算問題を解いてみよう【1ミリ秒は何ナノ秒】
- 秒(s)とナノ秒(ns)の変換(換算)の計算問題を解いてみよう【1秒は何ナノ秒】
- 秒(s)とマイクロ秒(μs)の変換(換算)の計算問題を解いてみよう【1秒は何マイクロ秒】
- 時間や分を小数を用いた表記に変換する方法
- km/h(キロメートル毎時)とm/min(メートル毎分)の変換(換算)方法 計算問題を解いてみよう
- m/minとmm/sec(mm/s)の変換(換算)方法 計算問題を解いてみよう
- m/s2とGの変換(換算)方法【メートル毎秒毎秒の計算】
- 加速電圧から電子の速度とエネルギーを計算する方法【求め方】
- 比電荷の求め方と求める理由【サイクロトロン運動と比電荷】
- ha(ヘクタール)とa(アール)の換算(変換)方法 計算問題を解いてみよう
- m2(平方メートル:平米)とa(アール)の換算(変換)方法 計算問題を解いてみよう
- m/s2とgal(ガル)の変換(換算)方法【メートル毎秒毎秒の計算】
- 数密度とは?水や電子の数密度の計算を行ってみよう【銅の電子数密度】
- 【丸棒の重量】円柱の体積と重量の求め方【鉄の場合】
- クーロン定数と誘電率εとの関係や単位【k=1/4πε】
- 電気容量の単位のファラッド(ファラド、F)とクーロン(C)、ボルト(V)の換算(変換)方法【静電容量の単位】
- ナノファラッド(nF)とマイクロファラッド(μF)の変換(換算)方法【計算問題】
- ピコファラッド(pF)とマイクロファラッド(μF)の変換(換算)方法【計算問題】
- ナノファラッド(nF)とピコファラッド(pF)の変換(換算)方法【計算問題】
- g/cm3とg/Lの変換(換算)方法 計算問題を解いてみよう
- g/ccとg/Lの変換(換算)方法 計算問題を解いてみよう
- ファラッド(F)とマイクロファラッド(μF)の変換(換算)方法【計算問題】(コピー)
- kg/m3とg/mm3の変換(換算)方法 計算問題を解いてみよう
- kg/m3とkg/mm3の変換(換算)方法 計算問題を解いてみよう
- MPa(メガパスカル)とatm(大気圧)の変換(換算)方法 計算問題を解いてみよう【MPaと標準大気圧】
- atm(大気圧)とTorr(トル)の変換(換算)方法 計算問題を解いてみよう【標準大気圧】
- Pa(パスカル)とTorr(トル)の変換(換算)方法 計算問題を解いてみよう
- mmhgとTorr(トル)の変換(換算)方法 計算問題を解いてみよう
- 【丸パイプ】パイプの体積と重量計算方法【鉄、ステンンレス、銅の場合】
- mmhg(ミリエイチジー)とhPa(ヘクトパスカル)の変換(換算)方法 計算問題を解いてみよう
- mmhg(ミリエイチジー)とmmh2O(ミリエイチツーオー)の変換(換算)方法 計算問題を解いてみよう
- mmhg(ミリエイチジー)とcmh2O(センチメートルエイチツーオー)の変換(換算)方法 計算問題を解いてみよう
- mmH2O(ミリエイチツーオー)とcmh2O(センチメートルエイチツーオー)の変換(換算)方法 計算問題を解いてみよう
- kPa(キロパスカル)とTorr(トル)の変換(換算)方法 計算問題を解いてみよう
- MPa(メガパスカル)とTorr(トル)の変換(換算)方法 計算問題を解いてみよう
- 一次反応における半減期の導出方法 半減期の単位や温度依存性【計算問題】
- 一次反応における反応速度定数の求め方や単位 温度・圧力依存性はあるのか【計算問題】
- 二次反応における半減期の導出方法 半減期の単位や温度依存性【計算問題】
- 二次反応における反応速度定数の求め方や単位 温度・圧力依存性はあるのか【計算問題】
- km2(平方キロメートル)とa(アール)の換算(変換)方法 計算問題を解いてみよう
- mol/Lとmol/m3の換算(変換)方法 計算問題を解いてみよう
- モル濃度(mol/L)と規定度nの違いと換算(変換)方法 計算問題を解いてみよう
- mol/Lとg/Lの換算(変換)方法 計算問題を解いてみよう
- mol/Lとg/mLの換算(変換)方法 計算問題を解いてみよう
- kPa(キロパスカル)とmmh2O(ミリエイチツーオー)の変換(換算)方法 計算問題を解いてみよう
- kPa(キロパスカル)とcmh2O(水柱センチメートル)の変換(換算)方法 計算問題を解いてみよう
- Pa(パスカル)とmmh2O(ミリエイチツーオー)の変換(換算)方法 計算問題を解いてみよう
- Pa(パスカル)とcmh2O(水柱センチメートル)の変換(換算)方法 計算問題を解いてみよう
- mol/Lとppmの変換(換算)方法 計算問題を解いてみよう
- mmhg(ミリメートルエイチジー)とcmhg(センチメートルエイチジー)の変換(換算)方法 計算問題を解いてみよう
- 圧平衡定数の求め方とモル分率(物質量比)との関係【四酸化二窒素(N2O4)と二酸化窒素(NO2)の問題】
- モル(mol)とモーラー(M)の違いと計算方法
- アンモニアの反応やエチレンの反応の圧平衡定数の計算方法【NH3とc2h4の圧平衡定数】
- MPaAとMPaGの違いと変換(換算)方法 計算問題を解いてみよう
- dm3(立方デシメートル)とm3(立方メートル)の換算(変換)方法 計算問題を解いてみよう
- dL(デシリットル)とL(リットル)の換算(変換)方法 計算問題を解いてみよう
- dL(デシリットル)とmL(ミリリットル)の換算(変換)方法 計算問題を解いてみよう
- dm3(立方デシメートル)とL(リットル)の換算(変換)方法 計算問題を解いてみよう
- dm3(立方デシメートル)とcm3(立方センチメートル)の換算(変換)方法 計算問題を解いてみよう
- cm3(立方センチメートル)とml(ミリリットル)の換算(変換)方法 計算問題を解いてみよう
- L(リットル)とmL(ミリリットル)の換算(変換)方法 計算問題を解いてみよう
- L/hとm3/hの換算(変換)方法 計算問題を解いてみよう
- L/h(リットル毎時)とL/min(リットル毎分)の換算(変換)方法 計算問題を解いてみよう
- L/hとL/sの換算(変換)方法 計算問題を解いてみよう
- ノルマルヘキサン(n-ヘキサン)やノルマルへプタンなどのノルマル(n)とは何を表しているのか【ノルマルパラフィン】
- イソプレン、イソブタン、イソヘキサンなどのイソの意味は?【イソプロピルアルコール等】
- L/hとm3/sの換算(変換)方法 計算問題を解いてみよう
- L/hとkg/hの換算(変換)方法 計算問題を解いてみよう
- L/minとm3/hの換算(変換)方法 計算問題を解いてみよう
- L/minとkg/sの換算(変換)方法 計算問題を解いてみよう
- 複合材料の密度の計算方法【密度の合成】
- 温度の単位とケルビン(K)と度(℃)の変換(換算)方法【絶対温度と摂氏の計算】
- パラフィンとは?イソパラフィンやノルマルパラフィンとの違い【アルカンとの関係性】
- メタンが無極性分子であり、アンモニアが極性分子である理由【電気陰性度との関係】
- ナフテンやシクロパラフィン、シクロアルカンの違いや特徴【化学式】
- アルカン、アルケン、シクロアルカン、シクロアルケンの定義と違い【シクロとは】
- 不飽和度nの計算方法【アルカン、アルケン、アルキンの不飽和度】
- ナフタレン(C10H8)の化学式・分子式・構造式・電子式・示性式・分子量は?
- プロペン(プロピレン:C3H6)の化学式・分子式・構造式・電子式・示性式・分子量は?
- ブタン(C4H10)の化学式・分子式・構造式・電子式・示性式・分子量は?
- ブタン(C4H10)とペンタン(C5H12)の構造異性体とその構造式
- ペンタン(C5H12)の化学式・分子式・構造式・電子式・示性式・分子量は?
- ヘキサン(C6H14)の化学式・分子式・構造式・電子式・示性式・分子量は?
- シクロプロパン(C3H6)の化学式・分子式・構造式・電子式・示性式・分子量は?
- シクロブタン(C4H8)の化学式・分子式・構造式・電子式・示性式・分子量は?
- 飽和炭化水素は分子量が大きく、分岐が少ない構造ほど沸点・融点が高い理由【アルカンと枝分かれ・表面積】
- 飽和炭化水素と不飽和炭化水素を区別する方法【炭化水素の分類】
- シクロペンタン(C5H10)の化学式・分子式・構造式・電子式・示性式・分子量は?
- シクロヘキサン(C6H12)の化学式・分子式・構造式・電子式・示性式・分子量は?
- ブタジエンとブテンやアルケンとの違い
- ブテン(C4H8)の化学式・分子式・構造式・電子式・示性式・分子量は?
- アルコール、アルデヒド、エステルの不飽和度の計算方法
- ブタジエン(C4H6)の化学式・分子式・構造式・電子式・示性式・分子量は?
- シクロプロペン(C3H4)の化学式・分子式・構造式・電子式・示性式・分子量は?
- ケトン基、アルデヒド基、カルボキシル基、カルボニル基の違い【ケトン、アルデヒド、カルボン酸とカルボニル基】
- アントラセン(C14H10)の化学式・分子式・構造式・電子式・示性式・分子量は?昇華性のある分子結晶で紫外線の照射により光二量化(光反応)を起こす
- プロピン(C3H6)の化学式・分子式・構造式・電子式・示性式・分子量は?プロピンへの水付加の反応ではアセトンが生成する
- ブチン(C4H6)の化学式・分子式・構造式・電子式・示性式・分子量は?ブチンの水付加の反応式
- 【SPI】順列や円順列の計算問題を解いてみよう
- ppm(ピーピーエム)と%(パーセント:ppc)を変換(換算)する方法 計算問題を解いてみよう【演習問題】
- 【SPI】損益算の計算を行ってみよう
- 【SPI】割合や比の計算を行ってみよう
- 【SPI】速度算(旅人算)の計算を行ってみよう【追いつき算】
- 【SPI】仕事算の計算を行ってみよう【3人・2人の場合の問題】
- 【SPI】流水算の計算を行ってみよう【練習問題】
- 【SPI】非言語関連(計算)の練習問題の一覧
- 【SPI】鶴亀算(つるかめ算)の計算を行ってみよう
- 【SPI】コインを用いた確率の計算問題を解いてみよう
- 【SPI】くじの確率の計算問題を解いてみよう
- 【SPI】サイコロの確率の計算問題を解いてみよう
- 【SPI】トランプの確率の計算問題を解いてみよう
- 【SPI】玉に関する確率の計算問題を解いてみよう【赤玉や白玉の問題】
- シクロペンテン(C5H8)の化学式・分子式・構造式・電子式・示性式・分子量は?
- シクロヘキセン(C6H10)の化学式・分子式・構造式・電子式・示性式・分子量は?
- 接触水素化(接触還元)とは?【アルケン、アルキンへの接触水素化】
- リンドラー触媒(Lindlar触媒)での接触水素化【アルキンからアルケンへ】
- シン付加とアンチ付加とは?シス体とトランス体の関係【syn付加とanti付加】
- 過酢酸の化学式・分子式・構造式・分子量は?
- 過硫酸の化学式・分子式・構造式・分子量は?
- 【Excel】インチ(inch)とセンチ(cm)の変換(換算)方法 計算問題を解いてみよう【1インチは何センチ】
- インチ(inch)とミリ(mm)の変換(換算)方法 計算問題を解いてみよう【1インチは何ミリ】
- インチ(inch)とメートル(m)の変換(換算)方法 計算問題を解いてみよう【1インチは何メートル】
- フィート(feet)とセンチ(cm)の変換(換算)方法 計算問題を解いてみよう【1フィートは何センチ】
- 三フッ化ホウ素(ボラン:BF3)の分子の形が三角錐ではなく三角形となる理由 結合角や極性【平面構造】
- ボラン(三フッ化ホウ素:BF3)の化学式・分子式・構造式・電子式・分子量は?
- 四塩化炭素(CCl4)の分子の形が正四面体となる理由 結合角と極性【立体構造】
- 四塩化炭素(CCl4)の化学式・分子式・組成式・電子式・構造式・分子量は?
- アセチレン(C2H2)とエチレン(C2H4)の分子の形と分子の極性が無い理由【無極性分子】
- ジクロロメタン(塩化メチレン)の分子構造(立体構造)は?極性を持つ理由は?【極性溶媒】
- ジクロロメタン(塩化メチレン)の化学式・分子式・組成式・電子式・構造式・分子量は?
- ブロモメタン(臭化メチル)の化学式・分子式・構造式・分子量は?
- 【SPI】年齢算の計算問題を解いてみよう
- 【SPI】植木算の計算問題を解いてみよう
- ジボラン(B2F6)の化学式・分子式・構造式・電子式・分子量は?
- クロロホルム(CHCl3:トリクロロメタン)の化学式・分子式・組成式・電子式・構造式・分子量は?
- クロロベンゼン(C6H5Cl)の化学式・分子式・組成式・電子式・構造式・分子量は?
- パラジクロロベンゼン(C6H4Cl2)の化学式・分子式・組成式・電子式・構造式・分子量は?
- アニソール(メトキシベンゼン:C7H8O)の化学式・分子式・組成式・電子式・構造式・分子量は?
- シラン(SiH4:モノシラン)の分子式・組成式・電子式・構造式・分子量は?分子の形は?
- ホスフィン(PH3:リン化水素)の分子式・組成式・電子式・構造式・分子量は?分子の形や極性は?
- 【SPI】列車のすれ違いや、トンネルの長さの計算問題を解いてみよう【電車と通過算】
- 【SPI】ベン図を利用して集合の問題を解いてみよう【3つのベン図】
- 圧力(P)と体積(V)をかけるとエネルギー(ジュール:J)となる理由【Pa・m3=J】
- kN/mm2とMPa(メガパスカル)の変換(換算)方法 計算問題を解いてみよう
- GPa(ギガパスカル)とMPa(メガパスカル)の変換(換算)方法 計算問題を解いてみよう
- GPa(ギガパスカル)とN/mm2の変換(換算)方法 計算問題を解いてみよう
- GPa(ギガパスカル)とkg/cm2(kgf/cm2)の変換(換算)方法 計算問題を解いてみよう
- GPa(ギガパスカル)とN/m2の変換(換算)方法 計算問題を解いてみよう
- GPa(ギガパスカル)とN/cm2の変換(換算)方法 計算問題を解いてみよう
- GPa(ギガパスカル)とkN/mm2の変換(換算)方法 計算問題を解いてみよう
- GPa(ギガパスカル)とkN/m2の変換(換算)方法 計算問題を解いてみよう
- ヨウ素と水素の反応の平衡定数の計算方法【平衡定数の単位】
- 分(min)を時間(h)の小数点の表記に変換する方法
- 時間と日(日数)を変換(換算)する方法【計算式】
- m/min(メートル毎分)とm/s(メートル毎秒)を変換(換算)する方法【計算式】
- 液体窒素と熱湯を混ぜるとどうなるのか
- m/minとmm/minを変換(換算)する方法【計算式】
- シクロヘキセンオキシド(C6H10O)の構造式は?水と反応し開環が起こる
- ジエチルエーテル(C4H10O)の構造式・示性式・化学式・分子式・分子量は?
- ブタノール(C4H10O)の化学式・分子式・構造式(構造異性体)・示性式・分子量は?
- プロパノール(C3H8O)の化学式・分子式・構造式(構造異性体)・示性式・分子量は?
- ブタノールの完全燃焼の化学反応式は?酢酸との反応式は?
- エチルメチルエーテル(C3H8O)の化学式・分子式・構造式・示性式・分子量は?
- メタノール(CH3OH)の完全燃焼の化学反応式は?生成する二酸化炭素の水の質量の計算方法
- メタン(CH4)の完全燃焼の化学反応式は?生成する二酸化炭素の水の質量の計算方法
- プロパン(C3H8)の完全燃焼の化学反応式は?生成する二酸化炭素の水の質量の計算方法
- N/m2とN/cm2の変換(換算)方法 計算問題を解いてみよう
- N/m2とN/mm2の変換(換算)方法 計算問題を解いてみよう
- ブタン(C4H10)の完全燃焼の化学反応式は?生成する二酸化炭素の水の質量の計算方法
- N/cm2とN/mm2の変換(換算)方法 計算問題を解いてみよう
- C3H8Oの分子式を持つ構造異性体の数とその構造式や名称(名前)は?
- C4H10Oの構造異性体の数とその構造式や名称(名前)は?
- 1gや1kgあたりの値段を計算する方法【重さあたりの単価】
- MB(メガバイト)、GB(ギガバイト)、TB(テラバイト)の変換(換算)方法 計算問題を解いてみよう
- 水を混合したときの温度を計算する方法【求め方】
- グルコース(ブドウ糖:C6H12O6)の完全燃焼の化学反応式【求め方】
- アルミニウム(Al)やマグネシウム(Mg)の完全燃焼の化学反応式【酸化アルミニウム、酸化マグネシウム】
- エチルメチルケトン(C4H8O)の化学式・分子式・構造式・示性式・分子量は?【危険物】
- ピリジン(C5H5N)の化学式・分子式・構造式・示性式・分子量は?【危険物乙四・甲種】
- ジエチルケトン(C5H10O)の構造式・化学式は?ヨードホルム反応を起こすのか?
- 酢酸やギ酸はヨードホルム反応を起こすのか【陰性】
- エタノールやメタノールはヨードホルム反応を起こすのか【陰性】
- アセトアルデヒドやホルムアルデヒドはヨードホルム反応を起こすのか
- 酢酸エチルはヨードホルム反応を起こすのか
- グラファイト(黒鉛)に導電性があり、ダイヤモンドは電気を通さない理由
- ジメチルエーテル(C2H6O)の構造式・示性式・化学式・分子式・分子量は?完全燃焼の反応式は?
- C2H6Oの分子式を持つ構造異性体の数とその構造式や名称(名前)は?
- ジメチルエーテル(C2H6O)の分子構造と極性がある理由
- C3H4の分子式を持つ構造異性体の数とその構造式や名称(名前)は?
- C4H8の構造異性体の数とその構造式や名称(名前)は?
- アシル基とアセチル基の定義と違い
- アセチル化の定義とエステル化との違い
- サリチル酸がアセチル化されアセチルサリチル酸となる反応式
- 酢酸ビニル(C4H6O2)の構造式・示性式・化学式・分子量は?
- スチレン(C8H8)の構造式・示性式・化学式・分子量は?付加重合によりポリスチレンが生成する反応式
- 塩化ビニル(クロロエチレ:C2H3Cl)の構造式・示性式・化学式・分子量は?
- プロピレン、ブタンの燃焼熱の計算問題を解いてみよう
- ビニロンの合成方法 酢酸ビニルの付加重合、アセタール化、けん化の反応式【ポリビニルアルコールやホルムアルデヒド】
- 酢酸とエタノールやアセチレンとの反応式
- アセトアニリドの化学式・分子式・構造式・分子量は?
- アニリンと塩酸の反応式(アニリン塩酸塩生成)やアニリン塩酸塩と水酸化ナトリウムの反応式
- アニリンと無水酢酸の反応式(アセトアニリド生成) 酢酸を使用しない理由は?
- カルシウムカーバイド(炭化カルシウム)の構造式・示性式・化学式・分子量は?
- 1mlや1Lあたり(リットル単価)の値段を計算する方法【100mlあたりの価格】
- 1mあたりの値段を計算する方法【メートル単価】
- Hz(ヘルツ)とs-1(1/s)を変換(換算)する方法【計算式】
- min-1(1/min)とs-1(1/s)の変換(換算)の計算問題を解いてみよう
- Hz(ヘルツ)とmin-1(1/min)変換(換の計算問題を解いてみよう
- min-1(1/min)とrpmの変換(換算)の計算問題を解いてみよう
- φは直径の寸法を表す記号 計算問題を解いてみよう【外径と内径との関係】
- rad/sとrpmの変換(換算)の計算問題を解いてみよう
- 図面におけるtの意味と使い方【板厚(厚み)】
- 音速と温度(気温)の式は?計算問題を解いてみよう
- 縮尺の計算、地図上の長さや実際の長さを求める方法
- Hz(ヘルツ)とrpmの変換(換算)の計算問題を解いてみよう
- Hz(ヘルツ)とrad/sの変換(換算)の計算問題を解いてみよう
- m/s(メートル毎秒)とrpmの変換(換算)の計算問題を解いてみよう
- kHz(キロヘルツ)とMHz(メガヘルツ)の変換(換算)の計算問題を解いてみよう
- GHz(ギガヘルツ)とMHz(メガヘルツ)の変換(換算)の計算問題を解いてみよう(コピー)
- GHz(ギガヘルツ)とkHz(キロヘルツ)の変換(換算)の計算問題を解いてみよう
- kcal/hとkW(キロワット)の変換(換算)方法 計算問題を解いてみよう
- MeV(メガ電子ボルト)とeV(電子ボルト:エレクトロンボルト)の換算(変換)方法 計算問題を解いてみよう
- MeV(メガ電子ボルト)とkeV(キロ電子ボルト)の換算(変換)方法 計算問題を解いてみよう
- MeV(メガ電子ボルト)とJ(ジュール)の換算(変換)方法 計算問題を解いてみよう
- kWh(キロワット時)とMWh(メガワット時)の変換(換算)方法 計算問題を解いてみよう
- kJ/molとkJ/kgの換算(変換)方法 計算問題を解いてみよう
- 周期と振動数(周波数)の変換(換算)の計算を行ってみよう【等速円運動】
- サリチル酸の構造式・化学式・分子式・分子量は?
- 安息香酸の構造式・化学式・分子式・分子量は?二量体の構造は?
- ブロモエタン(臭化エチル)の構造式・化学式・分子式・分子量は?
- cm-1(1/cm)とnmの変換(換算)の計算問題を解いてみよう
- cm-1(1/cm)とμmの変換(換算)の計算問題を解いてみよう
- cm-1(1/cm)とm-1(1/m)の変換(換算)の計算問題を解いてみよう
- ベクレル(Bq)とミリベクレル(mBq)の変換(換算)の計算問題を解いてみよう
- nm(波長)とev(エネルギー)の変換(換算)の計算問題を解いてみよう
- kL(キロリットル)とmL(ミリリットル)の換算(変換)方法 計算問題を解いてみよう
- kL(キロリットル)とm3(立方メートル)の変換(換算)方法 計算問題を解いてみよう
- kL(キロリットル)とcm3(立方センチメートル)の変換(換算)方法 計算問題を解いてみよう
- cal(カロリー)とWh(ワットアワー)の変換(換算)方法 計算問題を解いてみよう
- コンクリートでのm3(立米)とt(トン)の換算方法 計算問題を解いてみよう【密度、比重から計算】
- 1リットル(L)は何キログラム(kg)?【水、牛乳、ガソリン、油(灯油)、土、砂のキロ数】
- ミリオンやビリオンの意味は?10の何乗?100万や10億を表す【million,billion】
- クロロエタン(塩化エチル)の構造式・化学式・分子式・示性式・分子量は?エチレンと塩化水素からクロロエタンが生成する反応式
- g/cm3とt/m3の変換(換算)方法 計算問題を解いてみよう
- kg/Lとt/m3の変換(換算)方法 計算問題を解いてみよう
- kg/m3とt/m3の変換(換算)方法 計算問題を解いてみよう
- 数字の後につくKやMやGの意味や換算方法【キロ、メガ、ギガ】
- 木材においてm3(立米)とt(トン)を換算する方法 計算問題を解いてみう
- cm3(立方センチメートル)とcc(シーシー)の換算(変換)方法 計算問題を解いてみよう
- mm3(立方ミリメートル)とcc(シーシー)の換算(変換)方法 計算問題を解いてみよう
- kg/cm3とt/m3の変換(換算)方法 計算問題を解いてみよう
- kg/dm3とt/m3の変換(換算)方法 計算問題を解いてみよう
- アクリロニトリルの構造式・化学式・分子式・示性式・分子量は?重合したポリアクリロニトリルの構造は?
- アセトニトリルの構造式・化学式・分子式・示性式・分子量は?
- アクリル酸の構造式・化学式・分子式・示性式・分子量は?
- アクロレイン(アクリルアルデヒド)の構造式・化学式・分子式・示性式・分子量は?
- メタクリル酸の構造式・化学式・分子式・示性式・分子量は?
- メタクリル酸メチルの構造式・化学式・分子式・示性式・分子量は?
- mL(ミリリットル)とmm3(立方ミリメートル)の変換(換算)方法 計算問題を解いてみよう
- μL(マイクロリットル)とmm3(立方ミリメートル)の変換(換算)方法 計算問題を解いてみよう
- μL(マイクロリットル)とmL(ミリリットル)の変換(換算)方法 計算問題を解いてみよう
- μL(マイクロリットル)とdL(デシリットル)の変換(換算)方法 計算問題を解いてみよう
- 付加重合と縮合重合の違いは?
- フェノール(C6H5OH)の化学式・分子式・構造式・電子式・示性式・分子量は?
- ベンズアルデヒド(C7H6O)の化学式・分子式・構造式・示性式・分子量は?
- ブロモベンゼン(C6H5Br)の化学式・分子式・組成式・構造式・分子量は?
- 構造異性体、幾何異性体(シストランス異性体)、立体異性体の違いと分類方法
- 光学異性体、幾何異性体(シストランス異性体)の違いと覚え方
- 塩化ベンゼンジアゾニウムの化学式・構造式・示性式の書き方は?分子量はいくつか?
- ナフトールの化学式・構造式・分子式・示性式・分子量は?
- ベンジルアルコール(C7H8O)の化学式・分子式・構造式・示性式・分子量は?酸化されベンズアルデヒドになる時の反応式は?
- フェニル基とベンジル基の違いは?
- アルキル基と炭化水素基の違いは?
- ピクリン酸(トリニトロフェノール)の化学式・分子式・構造式・示性式・分子量は?
- ナトリウムフェノキシドの化学式・分子式・構造式・示性式・分子量は?
- グリシンの化学式・分子式・構造式・示性式・分子量は?
- アラニンの化学式・分子式・構造式・示性式・分子量は?
- トリニトロトルエンの化学式・分子式・構造式・示性式・分子量は?【TNT】
- アゾベンゼンの化学式・分子式・構造式・示性式・分子量は?光異性化の反応
- 図面におけるRの意味や書き方 内Rと外Rの違いやR面取りとは何か
- エチルベンゼン(C8H10)の化学式・分子式・構造式・分子量は?
- アゾ基とジアゾ基の違いは?
- ヒドラジンの化学式・分子式・構造式・分子量は?
- クロロプレン(C4H5Cl)の化学式・分子式・示性式・構造式・分子量は?クロロプレンゴムの構造式は?
- イソプレン(C5H8)の化学式・分子式・示性式・構造式・分子量は?イソプレンゴム(ポリイソプレン)の構造は?
- ベンゼンスルホン酸(C6H6O3S)の化学式・分子式・示性式・構造式・分子量は?
- 図面におけるCの意味や書き方 角度との関係
- ビニルアセチレン(C4H4)の化学式・分子式・示性式・構造式・分子量は?
- 図面におけるw・d・hの意味は【縦横高さの表記の意味】
- シクロヘキサノン(C6H10O)の化学式・分子式・構造式・示性式・分子量は?
- シクロヘキサノ―ル(C6H12O)の化学式・分子式・構造式・示性式・分子量は?
- リン酸の化学式・分子式・構造式・イオン式・分子量は?価数や電離式は?
- ポリテトラフルオロエチレン(PTFE)の化学式・分子式・構造式・示性式・分子量は?
- ポリアセタール(POM)の化学式・分子式・構造式・示性式・分子量は?
- ポリフッ化ビニリデン(PVDF)の化学式・分子式・構造式・示性式・分子量は?
- ポリフェニレンサルファイド(PPS)の化学式・分子式・構造式・示性式・分子量は?
- カルノーサイクルの一周とPV線図 仕事の導出方法【わかりやすく解説】
- ヒドロキシルアミン(NH2OH)の化学式・分子式・構造式・示性式・分子量は?危険物としての特徴<
- 等温変化における仕事の求め方と圧力との関係【例題付き】
- 等温変化での内部エネルギーと熱量の式
- 定圧変化での仕事(W=p⊿V)の求め方とPV線図【シャルルの法則 V/T=一定】
- C面取りや糸面取りの違いは【図面での表記】
- 逃げ加工とは?【フライスでの部材加工】
- テーパーと勾配の違い
- 正面図の選び方【正面図・平面図・側面図】
- アセトフェノン(C8H8O)の化学式・分子式・構造式・示性式・分子量は?
- プロピオンアルデヒド(C3H6O)の化学式・分子式・構造式・示性式・分子量は?
- 3キロは徒歩や自転車でどのくらいかかるのか【何歩でいけるか】
- 乳酸はヨードホルム反応を起こすのか【陽性】
- テトラヒドロフラン(THF:C4H8O)の化学式・分子式・構造式・示性式・分子量は?
- 人月と人日の変換(換算)方法 計算問題を解いてみよう【工数の単位】
- 人日と人時の変換(換算)方法 計算問題を解いてみよう【工数の単位】
- 片側公差と両側公差の違い【図面におけるマイナス0の公差とは】
- ヒドロキシ基とヒドロキシル基の違い【水酸基】
- ビニル基とアリル基の違いは?
- アリルアルコールの構造式・示性式・化学式・分子量は?
- 試作図と量産図の違いは?
- 段確、品確、量確とは?【製造プロセスと品質管理】
- バリやバリ取りとは?バリはなぜ発生するのか?【切削など】
- 板金のダボ加工(半抜き)とは?
- アリル基とアリール基の違いは?
- ターシャリーブチル基(tert-ブチル基)とは?ターシャリーブチルアルコールの構造
- コハク酸(C4H6O4)の構造式・示性式・化学式・分子量は?
- ジカルボン酸とは?
- 抜き勾配とは?基本的な角度やその計算方法・図面での指示について解説
- 勾配の1/50や1/100や1/1000とは?計算問題を解いてみよう【勾配の分数表記】
- 勾配のパーセントと角度の関係 計算問題を解いてみよう【10パーセントや20パーセントとは?】
- パーセント(百分率)とパーミル(千分率)の違いと変換(換算)方法【計算問題付き】
- イソプレンとブタジエンの違いは?
- エチレンが付加重合しポリエチレンとなる反応式は?構造式の違いは?
- 高級アルコールと低級アルコールの違いは?
- アルコールの級数と反応性(酸化)や沸点【第1級アルコールや第二級アルコールなどの違い】
- プロピレンが付加重合しポリプレピレンとなる反応式は?構造式の違いは?
- アルコールの炭素数と水溶性や極性との関係
- オクタン(C8H18)や一酸化炭素(CO)の完全燃焼の化学反応式は?【熱化学方程式】
- ppmとpptの変換(換算)方法 計算問題を解いてみよう【演習問題】
- mg/Lとmg/dLの変換(換算)方法 計算問題を解いてみよう【演習問題】
- mg/Lとg/mLの変換(換算)方法 計算問題を解いてみよう【演習問題】
- mg/Lとμg/mLの変換(換算)方法 計算問題を解いてみよう【演習問題】
- mg/Lとmg/mLの変換(換算)方法 計算問題を解いてみよう【演習問題】
- g/Lとmg/mLの変換(換算)方法 計算問題を解いてみよう【演習問題】
- mg/Lとmg/m3の変換(換算)方法 計算問題を解いてみよう【演習問題】
- 1年弱の意味は?1年強はどのくらい?【何か月くらい】
- 図面におけるフィレットの意味や寸法の入れ方【記号のRとの関係】
- 1時間弱の意味は?1時間強は何分くらい?【小一時間とは?】
- 10百万円はいくらか?100百万円は何円?英語での表記は?
- μV(マイクロボルト)とmV(ミリボルト)の変換(換算)方法 計算問題を解いてみよう
- 毎時と毎秒の変換(換算)方法 計算問題を解いてみよう
- 毎時と毎分の変換(換算)方法 計算問題を解いてみよう
- 毎秒と毎分の変換(換算)方法 計算問題を解いてみよう
- マイル毎時(mph)とメートル毎秒の変換(換算)方法 計算問題を解いてみよう
- インチ(inch)とフィート(feet)の変換(換算)方法 計算問題を解いてみよう【1フィートは何インチ】
- db(デシベル)と電圧比の関係 計算問題を解いてみよう【dbμv、dbmV、dbVとは?】
- Å(オングストローム)とμm(マイクロメートル)の換算(変換)方法 計算問題を解いてみよう
- Å(オングストローム)とcm(センチメートル)の換算(変換)方法 計算問題を解いてみよう
- μg(マイクログラム)とmg(ミリグラム)の変換(換算)方法 計算問題を解いてみよう
- μg(マイクログラム)とng(ナノグラム)の変換(換算)方法 計算問題を解いてみよう
- pg(ピコグラム)とng(ナノグラム)の変換(換算)方法 計算問題を解いてみよう【1ピコグラムは何ナノグラム】
- mg(ミリグラム)とng(ナノグラム)の変換(換算)方法 計算問題を解いてみよう【1ミリグラムは何ナノグラム】
- μgやmcgやmgの違いと変換(換算)方法
- 【MΩ】メガオームとメグオームの違い【読み方】
- A重油とB重油とC重油の違いは?流動点や動粘度や引火点との関係性
- 「電子と電荷の違い」と「電気と電荷の違い」
- 能動素子と受動素子の違い
- 電気回路と電子回路の違い 勉強する順番は?
- 流動点とは?流動点と凝固点の違い
- 煙点の意味やJISでの定義【灯油などの油】
- 原油の蒸留と分類(石油の精製) 石油と原油の違いや重質油と軽質油の違いは?
- ナフサとは?ガソリンとの違いは?簡単に解説
- 軽油・灯油・ガソリンの違いは?
- 軽油(ディーゼル)と重油の違いは?
- μΩ(マイクロオーム)とmΩ(ミリオーム)の換算(変換)方法 計算問題を解いてみよう
- uグラムとは何か【ug】
- ppmとmg/m3の変換(換算)方法 計算問題を解いてみよう【演習問題】
- mg/m3とμg/m3の変換(換算)方法 計算問題を解いてみよう【演習問題】
- 配管やパイプにおけるスケジュール(sch)とは?耐圧との関係性【sch40やsch80】
- 過負荷(オーバーロード)と過電流の違いは?過電圧との関係は?意味や原因、対処方法を解説
- 継電器(保護リレー)と遮断器(ブレーカー)の違いは?
- OCR(過電流継電器)、OVR(過電圧継電器)、UVR(不足電圧継電器)の意味と違いは?
- 電気設備におけるGCの意味は?AC回路とGC回路の違いは?
- ブレ―カーの「トリップ」の意味は?【電気関連の用語】
- kJ/hとkwの換算(変換)方法 計算問題を解いてみよう【発熱量の換算】
- 衝撃力(衝撃荷重)の計算方法【力積や速度との関係】
- J/hとw(ワット)の換算方法 計算問題を解いてみよう【熱量の変換】
- J/molとJ/kgの換算(変換)方法 計算問題を解いてみよう
- 原反とは?フィルムや生地やビニールとの関係
- 短絡と地絡の違いは?漏電との関係性
- LSA(低硫黄重油)とHAS(高硫黄重油)の違いは?AFOとの関係は?
- cal(カロリー)とw(ワット)の換算方法 計算問題を解いてみよう
- 石油におけるAPI度(ボーメ度)とは?比重との換算方法【原油】
- 1年は何週間なのか?52週?53周?54週?
- エタノールや塩酸は化合物(純物質)?混合物?単体?
- PFネジ(環用平行ねじ)とPTネジ(管用テーパねじ)の違いは?
- ブレーカーの極数(P)と素子数(E)とは?【3P3E・3P2E・2P2E・2P1E とは】
- 石油やドライアイスは混合物?純物質(化合物)?
- 電流、電圧、電力の変換(換算)方法 電圧が高いと電流はどうなる?
- 牛乳や岩石は混合物?純物質(化合物)?
- 電気におけるコモン線やコモン端子とは何か?【COM】
- SUSとSCSの違いは?【ステンレスの前置記号】
- 電線におけるSq(スケア:スクエア)の意味は?mmとの関係【ケーブル】
- 1φ3Wや3φ3Wや1φ2Wの意味と違い【単相3線や3相3線や3相3線】
- 図面における PCD(ピッチ円直径)の意味は?【ピッチ円半経との関係】
- SUS304とSUS316の違いは?【ステンレスの材質】
- 食酢や炭酸水は混合物?純物質(化合物)?
- 希釈液の作り方の計算方法は?濃度との関係は【問題付き】
- グルコースやスクロースは混合物?純物質(化合物)?
- 図面における繰り返しの寸法の表記方法【省略】
- 1ヶ月強は何日?1ヶ月弱はどのくらい?【1か月強と弱】
- 車で5分は徒歩で何分?自転車では?距離はどのくらい?【歩いて何分?】
- 1分強はどのくらい?1分弱の意味は?【2分弱や強は?】
- 車で10分は徒歩で何分?自転車では?距離はどのくらい?【歩いて何分?】
- 1メートル(m)強はどのくらい?1メートル(m)弱の意味は?【5分弱や強は?】
- 5キロは徒歩や自転車でどのくらいかかるのか【何歩でいけるか】
- インバーターとコンバーターの違いは?
- 10キロは徒歩や自転車でどのくらいかかるのか【何歩でいけるか】
- 1年足らずの意味は?1年余りはどのくらい?
- 1ヶ月余り(あまり)は何日?1ヶ月足らずはどのくらい?【1か月余りと足らず】
- 2キロは徒歩や自転車でどのくらいかかるのか【何歩でいけるか】
- rpmとrpsの変換(換算)方法は?計算問題を解いてみよう
- 4キロは徒歩や自転車でどのくらいかかるのか【何歩でいけるか】
- 大さじ1杯は小さじ何杯?【大さじと小さじの変換(換算)方法】
- 1週間強はどのくらい?1週間弱の意味は?【2週間弱や強は?】
- 10人強(10名強) は何人?10人弱(10名弱)の意味は?【20名弱や強は?】
- 砂糖水や食塩水は混合物?純物質(化合物)?
- ダイヤモンドや水は単体(純物質)?化合物?混合物?
- オゾンや石灰水は単体(純物質)?化合物?混合物?
- 氷やアンモニア水は単体(純物質)?化合物?混合物?
- ステンレスとメッキの違いは?
- 図面におけるサグリ(座繰り)やキリの表記方法は?【長穴の図面指示】
- 10円玉(銅)や銀の折り紙は電気を通すのか?
- 角パイプの重量計算方法は?【ステンレス(SUS)、鉄、アルミ】
- 1gや100gあたりのカロリーを計算する方法
- L(リットル)とgallon(ガロン)の換算方法 計算問題を解いてみよう
- アングルの重量計算方法は?【ステンレス(SUS)、鉄、アルミ】
- ネジやボルトのMの意味は?M3などの直径は何ミリ?何センチ?【M4、M5、M8、M10】
- アルミ板の重量計算方法は?【アルミニウム材の重量計算式】
- 鋼材(鉄板)の重量計算方法は?【鉄材の重量計算式】
- ステンレス板の重量計算方法は?【SUS304】
- 銅板の重量計算方法は?
- 錆びと酸化の違いは?酸化鉄との違いは?
- ポリプロピレン(PP:C3H6n)の化学式・分子式・構造式・分子量は?
- ポリエチレン(PE:C2H4n)の化学式・分子式・構造式・分子量は?【化学構造】
- 土砂や二酸化炭素は単体(純物質)?化合物?混合物?
- メタンやエタンなどの気体の密度と比重を求める方法【空気の密度が基準】
- プロパン(C3H8)や一酸化窒素(NO)などの気体の密度と比重を求める方法【空気の密度が基準】
- アンモニアやブタンなどの気体の密度(g/cm3やg/Lなど)と比重を求める方法【空気の密度が基準】
- 10分強はどのくらい?10分弱の意味は?【30分弱や強は?】
- アルゴンの化学式・組成式・分子式・構造式・分子量は?電子配置は?
- ヘリウムの化学式・組成式・分子式・構造式・分子量は?電子配置は?
- ネオンの化学式・組成式・分子式・構造式・分子量は?ネオンの電子配置は?
- 標高(高度)が100m上がると気温はどう変化するか【0.6℃】
- ニュートンメートル(n・m)とニュートン(n)の変換(換算)の計算方法【トルクの単位(n/mではない)】
- てこの原理を用いた計算方法【公式と問題】
- 塩化ナトリウムや酸化マグネシウムは単体(純物質)?化合物?混合物?
- 黒鉛(グラファイト)や赤リンや黄リンは単体(純物質)?化合物?混合物?
- ヘキサン(C6H14)の完全燃焼の化学反応式は?生成する二酸化炭素の水の質量の計算方法
- シクロヘキサン(C6H12)の完全燃焼の化学反応式は?生成する二酸化炭素や水の質量の計算方法
- wt%(重量パーセント)とat%(アトミックパーセント)の変換(換算)方法は?定義は?【原子比:原子パーセント】
- wt%(重量パーセント)とppm(ピーピーエム)の変換(換算)方法と違い
- 1個あたりの作業時間(個当たり工数)を計算する方法【作業時間の出し方】
- ニュートンメートル(n・m)とニュートンミリメートル(n・mm)の変換(換算)の計算方法【トルクの単位(n/mやn/mm2ではない)】
- ニュートンセンチメートル(n・cm)とニュートンミリメートル(n・mm)の変換(換算)の計算方法【トルクの単位(n/mやn/mm2ではない)】
- ニュートンメートル(n・m)とニュートンセンチメートル(n・cm)の変換(換算)の計算方法【トルクの単位(n/mやn/cmではない)】
- hPa(ヘクトパスカル)とkPa(キロパスカル)の変換(換算)方法 計算問題を解いてみよう【1hPaは何kPa?1KPaは何hPa?】
- hPa(ヘクトパスカル)とMPa(メガパスカル)の変換(換算)方法 計算問題を解いてみよう【1hPaは何MPa?1MPaは何hPa?】
- mS/mとμS/cmの換算(変換)方法は?計算問題を解いてみよう【ミリジーメンスパーメートルとマイクロジーメンスパーセンチメートル】
- cmhg(水銀柱センチメートル)とhPa(ヘクトパスカル)の変換(換算)方法 計算問題を解いてみよう
- S/mとS/cmの換算(変換)方法は?計算問題を解いてみよう【ジーメンス毎メートルとジーメンス毎センチメートル】
- mbar(ミリバール)とhPa(ヘクトパスカル)の変換(換算)方法 計算問題を解いてみよう
- mbar(ミリバール)とkPa(キロパスカル)の変換(換算)方法 計算問題を解いてみよう
- mbar(ミリバール)とbar(バール)の変換(換算)方法 計算問題を解いてみよう
- mh2O(maq)とmmh2O(mmaq)の変換(換算)方法 計算問題を解いてみよう
- mh2O(水柱メートル)とPa(パスカル)の変換(換算)方法 計算問題を解いてみよう
- 車で3分は徒歩で何分?自転車では?距離はどのくらい?【歩いて何分?】
- mh2O(水柱メートル)とkPa(キロパスカル)の変換(換算)方法 計算問題を解いてみよう
- mh2O(水柱メートル)とMPa(メガパスカル)の変換(換算)方法 計算問題を解いてみよう
- mh2O(水柱メートル)とhPa(ヘクトパスカル)の変換(換算)方法 計算問題を解いてみよう
- mbar(ミリバール)とPa(パスカル)の変換(換算)方法 計算問題を解いてみよう
- マグネシウムイオン・硫化物イオンと同じ電子配置は?
- 何倍かを求める式の計算方法【分数での計算も併せて】